Потери - иод
Cтраница 1
Потери иода в этом процессе определяются образованием небольших количеств органических иодидов, отлагающихся в виде темного налета в конце реактора при выходе газа из печи. [1]
Потери иода распределяются по стадиям производства примерно следующим образом. С отработанной буровой водой теряется при чистых водах около 5 %, а при загрязненных водах 10 - 15 % иода. Вследствие механических потерь угля на стадии адсорбции теряется до 2 % иода. При отмывке угля потери иода составляют 2 - 4 % и столько же теряется при выделении иода. [2]
Потери иода распределяются по стадиям производства примерно следующим образом. С отработанной буровой водой теряется при чистых водах около 5 %, а при загрязненных водах 10 - 1о % иода. Вследствие механических потерь угля на стадии адсорбции теряется до 2 % иода. При отмывке угля потери иода составляют 2 - 4 % и столько же теряется при выделении иода. [3]
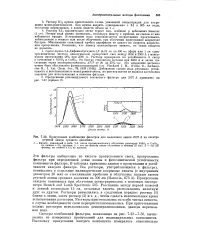 |
Пропускание комбинации фильтров для выделения линии 2537 А из спектра ртутной лампы среднего давления. [4] |
Потери иода можно уменьшить, используя кювету с пробкой, но совсем от них избавиться трудно. Исчезновение иода сопровождается возрастанием пропускания, наблюдаемым в темноте или после облучения; при облучении пропускание возрастает быстрее. Обмазывание стеклянной пробки парафином не влияет на скорость возрастания пропускания. Возможно, что кювету целесообразно запаять, но таких попыток не делалось. [5]
Потери иода вследствие испарения особенно легко могут происходить, когда концентрация иодида слишком низка и в системе содержится твердый иод. Чтобы уменьшить концентрацию свободного иода до величины ниже предела насыщения, в растворе следует иметь достаточное количество иодида. Опасность испарения свободного иода увеличивается при выделении газов ( например, двуокиси углерода при деаэрации) и при нагревании. Поэтому определения следует проводить, пользуясь холодными растворами. [6]
 |
Данные, характеризующие присоединение иода к ненасыщенным соединениям в условиях иодометрического анализа пероксидов. [7] |
Поскольку потери иода приблизительно пропорциональны начальной его концентрации в растворе, отсутствие потерь его при наличии иодида, несомненно, можно объяснить образованием инертного трииодид-иона и в результате этого малой концентрацией свободного иода. [8]
Бочьшую часть потерь на стадии десорбций составляют потери иода о отмытых угней, что объиснпегвч непоиной от - мнвной йода перед ныгцузкой их из котнов. Зяя снижения этик потерь необходимо довести содержание иода в утпя. [9]
Источники погрешностей в иодометрических методах следующие: 1) потери иода вследствие летучести; 2) окисление иодид-иона кислородом воздуха; 3) изменение характеристик стандартных растворов тиосульфата в процессе их хранения и использования; 4) изменение стехиометрии реакции иода с тиосульфатом при титровании щелочных растворов; 5) относительно медленная реакция окисления иодидов окислителями; 6) адсорбция элементного иода поверхностно-активными веществами и некоторыми осадками, получающимися в процессе иодометрического титрования. Поэтому в конце титрования следует тщательно перемешивать титруемый раствор, содержащий осадок. [10]
При титровании раствора обычно ощущается запах иода, однако потери иода при этом незначительны. [11]
Если раствор имеет чересчур кислую реакцию, при кипячении могут происходить потери иода; если раствор слишком щелочной, то образуется бромат. Шулек и Эндреи предложили для удаления избытка хлора добавлять цианид калия, который связывает хлор в хлор циан CNC1 - вещество, неактивное по отношению к иодиду. [12]
Результаты этого титрования являются ориентировочными, так как в процессе опыта возможны потери иода за счет его летучести. [13]
При количественных определениях с помощью иода возможны два источника погрешностей: 1) потери иода вследствие его летучести; 2) окисление иодида кислородом воздуха. [14]
Увеличение концентрации KJ приводит к смещению равновесия в правую сторону, что уменьшает потери иода от испарения. [15]
Страницы: 1 2 3 4