Потери - иод
Cтраница 2
Повышение температуры и концентрации смеси HJ H2SO4 в адсорбционной башне выше указанного предела увеличивает потери иода из-за роста давления пара йодистого водорода над раствором. Получающиеся после выделения иода маточные рассолы, содержащие 25 - 35 г / л НС1 и 80 - 120 г / л H2SO4, используют для подкисления исходной буровой воды или для других целей. [16]
При количественных определениях с помощью иода обычно бывают два источника ошибок: 1) потери иода вследствие его летучести; 2) окисление иодида кислородом воздуха. [17]
Повышение температуры и концентрации смеси HI и Нй5Од в адсорбционной башне выше указанного предела увеличивает потери иода из-за роста давления пара йодистого водорода над раствором. [18]
Повышение температуры и концентрации смеси HI и H2SO4 в адсорбционной башне выше указанного предела увеличивает потери иода из-за роста давления пара йодистого водорода над раствором. Получающиеся после выделения иода маточные рассолы, содержащие 25 - 35 г / л НС. [19]
После десорбции для фиксации 1 - - ионы окисляют гипохлоритом натрия до элементарного иода; это предотвращает потери иода на последующей стадии сорбции. [20]
Осторожно отвешивают приблизительно 0 5 г иода в стаканчик для взвешивания или другой сосуд, предохраняющий от потери иода из-за улетучивания во время взвешивания или во время переноса в сосуд для титрования и не изменяющий своего веса вовремя взвешивания. [21]
Хранение титрованных растворов иода в темном и прохладном месте в склянке из темного стекла с притертой пробкой уменьшает потери иода. Хранение растворов иода в склянках с резиновыми или корковыми пробками недопустимо. [22]
Иод можно также выделять из щелоков при пропускании через них хлора 21 - 4 - С12 2СГ 12; однако при этом возможны потери иода, так как в случае избытка хлора часть иода окисляется до иодата, который остается в рассоле. [23]
Иод можно также выделять из щелоков при пропускании через них хлора 21 - 4 - С12 2СГ - 12; однако при этом возможны потери иода, так как в случае избытка хлора часть иода окисляется До иодата, который остается в рассоле. [24]
Если содержание KJ в растворе достигает 4 % и если температура в лаборатории не выше 25, то за несколько минут, которые требуются на одно титрование, потери иода от испарения настолько малы, что ими можно пренебречь. [25]
Найдено, что без стабилизатора KI полностью разлагается за 2 - 3 месяца, а в присутствии 1 % Na2S203 от веса KI ( или 0 00001 % Na2S203 от веса соли) потери иода не происходит в течение 6 мес. [26]
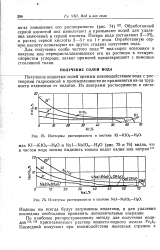 |
Изотермы растворимости - в системе KI - КЮ3 - Н2О.| Изотермы растворимости в системе Nal - NaIO3 - Н2О. [27] |
Обработанный серной кислотой иод измельчают и промывают водой для удаления включений и серной кислоты. Потери иода составляют 2 - 3 %, а расход серной кислоты 2 - 3 г на 1 т иода. Отработанную серную кислоту используют на других стадиях получения иода. [28]
 |
Изотермы растворимости в системе KI - КЮ3 - Н2О.| Изотермы растворимости в системе Nal - NaIO3 - Н2О. [29] |
Обработанный серной кислотой иод измельчают и промывают водой для удаления включений и серной кислоты. Потери иода составляют 2 - 3 %, а расход серной кислоты 2 - 3 т на I т иода. Отработанную серную кислоту используют на других стадиях получения иода. [30]
Страницы: 1 2 3 4