Замена - остаток
Cтраница 1
Замена остатка Туг2 гистидином [ Шз2 - Ьуз8 - вазопрессин ( IX) ] [896] приводит к полной потере биологической активности ( 0 01 / мг), что свидетельствует о существенной роли оксифенильной или фенильной группы остатка в положении 2 для проявления физиологического действия. [1]
Замена остатка Glu ( NH2) 4 на аспарагин подтверждает, что, как и в ряду окситоцина, присутствие в положении 4 остатка глутамина не обязательно для проявления биологической активности. Asp ( NH2) 4 - Lys8 - Ba3onpeccHH ( XXII) [2650] имеет в два раза более высокую антидиуретическую активность, чем Lys8 - вазопрессин, наряду с несколько пониженной вазопрессорной активностью ( ср. Однако эти данные не подтверждены исследованиями, выполненными в другой лаборатории [ 291 а ]; при этом было найдено, что прессорная активность Asp ( NH2) 4 - Ьуз8 - вазопрессина равна 54 12, а антидиуретическая - 24 3 / мг. [2]
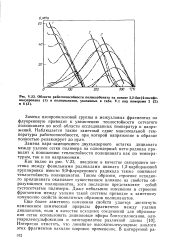 |
Области работоспособности поликарбоната на основе 2 2-бис ( 4-оксифе-нил пропана ( 1 и полицианатов, указанных в под номерами 2 ( 2 и 8 ( 3. [3] |
Замена пара-замещешгого двухъядерного остатка дицианата между узлами сетки полимера на одноядерный мета-радикал приводит к понижению теплостойкости полицианата как по температурам, так и по напряжениям. [4]
Интересные результаты получены при замене изолейцинового остатка в положении 3, играющего существенную роль в проявлении биологической активности, на остатки других аминокислот. Активность соответствующих аналогов убывает в следующем порядке: IleuValLeuPheTyrTry. Рудингер и Крейчи [1856] исследовали зависимость между вводимой дозой и последующим эффектом на примере alleu3 -, NVal3 -, Val3 -, NLeu3 - и Ьеи3 - окситоцинов. Авторам удалось показать, что уменьшение активности аналогов, замещенных в положении 3, объясняется снижением эффективности связывания с рецептором. Окситоцин ( XX) [167, 297, 1855, 1856] при испытаниях in vitro на матке крысы и на кровяное давление у птиц в восемь раз менее активен, чем окситоцин. Таким образом, для Уа13 - окситоцина наблюдается более избирательная окситотическая активность, чем для окситоцина, что проявляется более четко в опытах in vivo, чем in vitro. Интересно, что замена изолейцинового остатка на какую-либо другую ароматическую аминокислоту ( Туг3 - оксито-цин XIX [166, 288] и Тгу3 - окситоцин XVIII [166, 896]) приводит к практически неактивным соединениям. [5]
Изменение суммарного заряда HbS, связанное с заменой остатка глютаминовой кислоты на валин, приводит и к изменению электрофоретической подвижности HbS по сравнению с подвижностью НЬА. [6]
Следует отметить большую разницу, к которой приводит замена остатка Arg9 на His9, в гипотензивной ( 1 / 20) и в бронхосокращающей ( менее 1 / 2000) активности в опытах на морских свинках. Существенное различие наблюдается и в действии этого соединения на кровяное давление у морских свинок и кроликов. Высокая гипотензивная активность Сиэ-брадикинина свидетельствует о важности структурно-пространственных факторов, поскольку в этом случае сильноосновной остаток аргинина заменен на нейтральный, но близкий по своей структуре остаток цитруллина. Однако большая по сравнению с С119 - брадикинином активность соответствующего Ьуз9 - соединения говорит о том, что основность С-концевой аминокислоты играет более существенную роль. В ряду Lys9 - Ьуз1 - Ьу81 - Ьу59 - брадикининов активность уменьшается слева направо; точно такая же закономерность наблюдается и у соответствующих производных цитруллина. Правда, дез - ( Аге - брадикинин ( LIII) [ 1617, 1617а ] обладает большей активностью, чем дез - ( А 9) - брадикинин ( LIX) [ 1617, 597а ], но этот факт не опровергает приведенного выше положения, поскольку отсутствие какой-либо аминокислоты дает совсем не тот эффект, что ее замена на другую аминокислоту. [7]
В этом случае, очевидно, сначала идет замена четвертичного остатка, а потом - перегруппировка Стивенса. [8]
Ранее нами было отмечено ( 6), что замена алифатического остатка ( R) анилида на фенильное кольцо сопровождается снижением ингибирования реакции Хилла. В отличие от этого, М - ( 3-три-фторметилфенил) - 2, 3, 4-трихлорбензамид активно подавлял реакцию Хилла. [9]
Удлинение цени конъюгации в аминной части молекул салицил-альанилинов при замене N-фенпльного остатка га-дифенилильным, и-терфенилильным и другими, а также удвоение молекул ( бисазоме-тины) вызывают длинноволновое смещение максимумов флуоресценции одновременно с длинноволновым сдвигом полосы поглощения. Пространственные затруднения в ядре дифенила, разобщение азоме-тиновых систем мостиками, прерывающими цепь сопряжения, мета-расположение азометиновых групп в центральном ароматическом ядре [42, 44, 66] вызывают противоположный эффект: максимумы флуоресценции сдвигаются в коротковолновую область спектра. Структурные изменения в молекулах моно - и бисазометинов в значительно меньшей степени сказываются на спектрах люминесценции салицилальпроизводных, чем на спектрах 2-гидрокси - 1-нафтальпро-изводных. [10]
Вместе с тем, большой интерес представляют изыскания, направленные к замене метилуретанового остатка на другие группировки, например сложноэфирную31а, амидиновую и пр. [11]
Установлено, что при метаболизме происходит замена атомов хлора на гидроксил, замена остатка фенилугольной кислоты на остаток глюкуроновой кислоты и окисление С-4 и С-6 до соответствующих карбонильных соединений с дальнейшим размыканием цикла. [12]
Однако это объяснение не очень убедительно; вполне возможно, что в данном случае мутаротация вызвана химической реакцией - заменой остатка ж-аминобензойной кислоты в основании Шиффа на остаток () - а-фенилэтиламина. [13]
Было исследовано влияние изменения строения углеводородного радикала, связанного с фосфором, эфирного остатка, алкильного радикала при азоте и замены фосфорильного остатка тиофосфорильным на пестицидные свойства полученных соединений. [14]
Оказалось, что и прямое действие на ферроценилборную кислоту медных ( Си) солей карбоновых кислот ( 17), а также медных N-производ-ных, подобных фтальимиду меди ( 18), приводит к замене остатка борной кислоты на анион. [15]
Страницы: 1 2 3