Экваториальный заместитель
Cтраница 1
Экваториальный заместитель не может легко вступать в реакцию 5 2, так как противоположная сторона атома углерода экранирована остальной частью цикла ( ср. [1]
 |
Конформации ( констелляции циклогексанового кольца. [2] |
При этом экваториальный заместитель переходит в аксиальное положение, ч наоборот. [3]
Соединения с экваториальными заместителями в общем более устойчивы, чем их изомеры с аксиальными заместителями. Аномалии, наблюдающиеся у некоторых продуктов распада дитерпеноидов и тритерпеноидов, побудили Бартона ( Barton, 1953а, примечание 64; 1953Ь) к более детальному рассмотрению различных типов полизамещенных циклогексанов. [4]
В циклогексановом кольце экваториальный заместитель поглощает при более высоких частотах, чем соответствующий аксиальный. [5]
Соединения с обоими экваториальными заместителями ( LXIXA) неспособны к таким реакциям элиминирования. [6]
В общем, можно сказать, что экваториальные заместители более доступны атаке и вступают в реакции с большей скоростью. [7]
В процессе этого мнимого вращения одни из экваториальных заместителей, называемый опорным лигандом ( в нашем случае обозначен цифрой 5) остается в экватор альном положении, в то время как другие лиганды формируют собой основание воображаемой тетрагональной пирамиды за счет искажения валентных углов. Валентный угол между связями 1 - Р-2 уменьшается от 180 до 120, а между связями З - Р-4 увеличивается от 120 до 180, т.е. апикальные лиганды 1 и 2 в конце концов займут экваториальные, а экваториальные лиганды 3 и 4 - апикальные положения. [8]
В процессе этого мнимого вращения один из экваториальных заместителей, называемый опорным лигандом ( в нашем случае обозначен цифрой 5), остается в экваториальном положении, в то время как другие лиганды формируют собой основание воображаемой тетрагональной пирамиды за счет искажения валентных углов. Валентный угол между связями 1 - Р-2 уменьшается от 180 до 120, а между связями З - Р-4 увеличивается от 120 до 180, т.е. апикальные лиганды 1 и 2 в конце концов займут экваториальные, а экваториальные лиганды 3 и 4 - апикальные положения. [9]
Недавно было рассмотрено также взаимодействие между двумя экваториальными заместителями в положениях 4 5 у соединений типа транс-анти-транс-пергидрофенантрена ( например, между заместителями в 1 [ 3 - и На - положениях соединения XLVI. В результате такого отталкивания аксиальный заместитель может в некоторых случаях оказаться более устойчивым, чем его экваториальный эпимер. В работе Эймса с соавторами ( Ames, Beton, Bowers, Hals all, Jones, i954) рассмотрены некоторые 18-а-тритерпеноиды с метильной ( и гидроксильной) группами в положении 19 ( нумерацию ср. [10]
Метилциклогексан может существовать либо в конформаций с экваториальным заместителем, либо в конформаций с аксиальным заместителем, обе конформаций находятся в быстро устанавливающемся равновесии между собой. Константа равновесия соответствует содержанию в смеси - 95 % экваториального и - 5 % аксиального метилциклогексанов; свободная энергия перехода ( аксиальный - - экваториальный), AG, равна - 7 5 кДж / моль. Предпочтительность экваториальной ориентации для метильного заместителя является общей чертой для монозамещенных циклогексанов. [11]
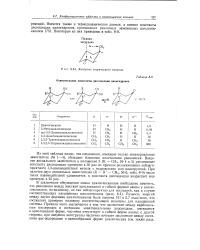 |
Контроль стерического подхода. [12] |
Из этой таблицы видно, что соединения, имеющие только экваториальные заместители ( № 1 - 3), обладают близкими константами равновесия. Введение аксиального заместителя в положение 3 ( R СН3 № 4 и 5) увеличивает константу диссоциации примерно в 30 раз по причине возникновения неблагоприятного 1 3-взаимодействия метила с гидроксилом или циангруппой. При наличии двух аксиальных заместителей ( R R СН3 № 6, табл. 8 - 9) число таких взаимодействий удваивается, и константа диссоциации возрастает еще примерно в 25 раз. [13]
Равновесие становится менее выгодным, если в диаксиальном изомере присутствует экваториальный заместитель при С-3, так как в результате эпимеризации этот заместитель займет сик-аксиалъное положение по отношению к одному из атомов брома. [14]
Каждый конформационный изомер этого соединения имеет один аксиальный и один экваториальный заместитель. Так как обе формы одинаково устойчивы, половина молекул существует в одной форме, а половина - в другой. [15]
Страницы: 1 2 3 4