Стереохимическое представление
Cтраница 3
Несравнимо проще объясняются случаи присоединения по месту кратной связи в ягрсшс-положении с точки зрения стереохимических представлений Вернера. Не считая возможным игнорировать многочисленные, установленные Михаэлем, факты транс-щтсоединения, Вернер [20] еще н 1904 г. указывал на несовместимость этих явлений с обычными стерео-химическими представлениями и рекомендовал крайнюю осторожность при определении конфигурации геометрических изомеров на основании реакции присоединения. В противоположность Михаэлю, Вернер полагал, однако, что стереохимически можно представить себе и транс - присоединение, если только отрешиться от формул и моделей, основанных на обычных представлениях о валентности. [31]
 |
Число публикаций по полному синтезу стероидов. [32] |
Следующий этап истории полного синтеза, который приходится на 50 - е годы, был связан с развитием новых стереохимических представлений, с разработкой специфических реакций, обеспечивших возможность направленного формирования центров асимметрии, и, наконец, с резким увеличением интереса к полному синтезу стероидов, вызванным широким внедрением их в медицинскую практику. В этот период, начавшийся в 1951 г., когда группы Робинсона ( схемы 56, 57, 59) и Вудворда ( схемы 109, НО) опубликовали работы о полном синтезе андростерона, холестерина ( 8) и кортизона ( 6), был осуществлен полный синтез всех неароматических стероидов. [33]
Большой победой координационной теории было получение в 1907 г. Вернером виолеосоли состава [ CofNHsKCyX, чем экспериментально еще раз подтвердились его стереохимические представления. До этого Иергенсен получил два комплексных соединения кобальта состава СоХз СгЩЫгЩ), или СоХз - 2Еп, в которых две молекулы этилендиамина замещают четыре молекулы аммиака. Соли одного ряда окрашены в зеленый цвет и называются празеосолями, соли другого ряда, получающиеся нагреванием с водой солей первого ряда, - фиолетового цвета, почему получили название виолеосолей. [34]
В настоящей книге мы изложим историю, пожалуй, основного направления в кинетике органических реакций - историю учения о связи строения органических молекул ( в рамках классических электронных и стереохимических представлений) с их реакционной способностью в период с 60 - х годов XIX в. Выбор нижнего хронологического предела обусловлен появлением первых работ по установлению связи между строением и реакционной способностью молекул, а опубликованная в 1941 г. монография Глесстона, Лейдлера и Эйрин-га Теория абсолютных скоростей реакций [21] явилась достойным завершением большого и интересного периода создания предпосылок для современного бурного развития кинетики органических реакций. [35]
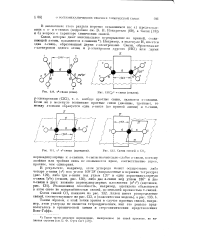 |
Схема слнзсй в СО.. [36] |
Таким образом, с этой точки зрения в случае кратных связей, например, атом углерода не является тетраэдрическим, как это раньше предполагалось в органической химии и стереохимических представлениях Вант-Гоффа. [37]
Предлагаемая ниже система обозначений пространственных изомеров является попыткой решить этот вопрос не для отдельных, частных случаев, как это обычно делалось до сих пор, а для всех мыслимых возможностей путем единого подхода, вытекающего из бутлеровской теории химического строения и дополняющих ее стереохимических представлений. [38]
Некоторые исследователи [37, 86] полагают, что наряду с указанными выше существуют кислоты других степеней гидратации и полимеризации, например моно - и диметакислота ( НР03 и Н2Р2Ов), ультрафосфорные кислоты ( Н2Рв01в, Н4Р6017) и др. Возможность существования подобных кислот вызывает обоснованные сомнения, так как их предполагаемые структуры прежде всего не соответствуют современным стереохимическим представлениям. [39]
Хотя вряд ли можно сомневаться в том, что олефины покидают поверхность во время гидрогенизации ароматического углеводорода, все же эти представления оспаривались. Стереохимические представления требуют, чтобы большая часть ( 50 %) ароматического углеводорода восстанавливалась через десорбированный циклогексен; однако Хартог и Цвитеринг [103 ] на основании кинетического анализа пришли к выводу, что эта доля невелика. [40]
Были открыты и нашли объяснение случаи стереоизомерии молекул, не имеющих асимметрических атомов углерода. Стереохимические представления были распространены на соединения других элементов помимо углерода. [41]
Согласно старому стереохимическому представлению ( см. выше), любое присоединение по двойной связи должно происходить по одну и ту же сторону двойной связи и, следовательно, являться цмс-присоединением. [42]
Уже простейшие рассуждения с учетом стереохимических представлений подсказывают, что введение каких-то заместителей, затрудняющих а-итнку карбонильной связи, должно увеличить выход t - отинилииоморов, сведение жи их к минимуму должнс; увеличивать долю а-этинильн. Поскольку принципиально можно достичь полной с-экранизации карбонильной связи ( например, я-заместителями положения 3), то практически можно направить реакцию по пути преимущественного или дажр исключительного образования е-изомеров. Иначе обстоит дело с е-экранированием: достичь полной е-изолядии принципиально невозможно, а следовательно, даже: в лучшем случае в результате реакции должна получаться смесь е - и а-изомеров, естественно, с преобладанием последнего. [43]
По-видимому, независимо от Клауса, десять лет спустя, аналогичные идеи ( но с использованием совершенно конкретной модели) развил Вернер. Выступая против общепринятой теории валентности и стереохимических представлений, Вернер прибегает к шаровой модели атома. В этом случае сродство есть сила притяжения, действующая от центра атома равномерно ко всем частям его шарообразной поверхности [ 50, стр. Часть сродства атома, потребляемая при возникновении связи, образует на шарообразной поверхности больший или меньший круг. В соединении CR4, если R - одинаковы, они занимают на шарообразной поверхности одинаковые связевые поверхности и расположены сами в углах правильного тетраэдра. Если четыре R не одинаковы, они располагаются в углах неправильного тетраэдра, и отсекаемые этими R части шаровой поверхности атома углерода отличаются по величине друг от друга. Если, например, какой-либо заместитель особенно прочно связан с атомом углерода, то он занимает относительно большую часть связевой поверхности, уменьшая, таким образом, части поверхности, приходящиеся на другие связи, и, следовательно, ослабляя их. [44]
Килиани и Эмиль Фишер начинают свои фундаментальные исследования, завершившиеся в 90 - х годах прошлого столетия установлением строения простейших углеводов. Решающее влияние на развитие химии углеводов оказали стереохимические представления Вант-Гоффа, причем развитие стереохимии также было неразрывно связано с химией углеводов; экспериментальный материал, почерпнутый из химии углеводов, сыграл очень важную роль в развитии основных положений стереохи-мической теории. [45]
Страницы: 1 2 3 4