Средняя валентность
Cтраница 2
Анодный ток вызывает в этом случае ( в суммарном процессе) обратимую отдачу атомов металла ( Me Mez ze -) покрывающему слою с одновременным повышением средней валентности вещества слоя. [17]
Подобно хрому, марганец при низших валентностях образует соединения основного характера, а его соединения с высшей валентностью обладают кислотным характером; в соединениях марганца со средней валентностью основные окислы постепенно переходят к кислотам. [18]
Показано, что при взаимодействии А1 ( С2Н5) 3, А1 ( С2Н5) 2С1 и А1 ( С2Н5) С12 с четыреххлористым ванадием его восстановление протекает практически до постоянной средней валентности, колеблющейся в пределах 2 5 - 3 в течение первых 10 мин. При этом с увеличением числа алкильных групп в алюминийорганическом соединении его восстановительная способность также повышается. При восстановлении VC14 алкилалюминийгалогенидами образуются различные продукты восстановления, тип и количество которых зависят от введенного алкилалюминийгалогепида. При восстановлении VC14 этилалюминийдихлоридом наряду с объемистым осадком, состоящим преимущественно из соединений V3, образуются растворимые продукты реакции, в которых содержится в основном двухвалентный ванадий. В осадке, в частности, имеется VC13, содержащий еще значительные количества алюминийорганического соединения или А1С13 ( в виде комплекса), которые лишь частично могут быть удалены органическими растворителями. В растворимой части с о-держатся хлористые соединения двухвалентного ванадия, связанные в виде комплексов с алкилалюминийдихлоридом или А1С13, и избыток алюминийоргапического соединения. [19]
Показано, что при взаимодействии А1 ( С2Н5) 3, А1 ( С2Н6) 2С1 и А1 ( С2Н5) С12 с четыреххлористым ванадием его восстановление протекает практически до постоянной средней валентности, колеблющейся в пределах 2 5 - 3 в течение первых 10 мин. При этом с увеличением числа алкильных групп в алюминийорганическом соединении его восстановительная способность также повышается. При восстановлении VC14 алкилалюминийгалогенидами образуются различные продукты восстановления, тип и количество которых зависят от введенного алкилалюминийгалогенида. При восстановлении VC14 этилалюминийдихлоридом наряду с объемистым осадком, состоящим преимущественно из соединений V3, образуются растворимые продукты реакции, в которых содержится в основном двухвалентный ванадий. В осадке, в частности, имеется VC13, содержащий еще значительные количества алюминииорганического соединения или А1С13 ( в виде комплекса), которые лишь частично могут быть удалены органическими растворителями. В растворимой части с о-держатся хлористые соединения двухвалентного ванадия, связанные в виде комплексов с алкилалюминийдихлоридом или А1С13, и избыток алюминииорганического соединения. [20]
В [12], [15], [32] было указано, что периодические изменения атомного номера связаны с закономерным изменением числа холостых электронов, что в свою очередь должно быть связано с симбатным ходом энергий сублимации простых веществ с образованием атомного пара и со средней валентностью тех же элементов по хлору и фтору. [21]
Для опытов брались навески окислов по 0.1 - 0.2 г, которые сплавлялись с 3 г пиросульфата калия. При расчетах средней валентности окислы принимались за стопроцентные продукты. [22]
Химические методы используют для определения валентности примесных атомов при условии, что основная масса кристалла растворяется без особых осложнений. Так, среднюю валентность марганца в люминесцентных кристаллах, активированных марганцем, устанавливают растворением кристалла в кислоте, содержащей йодистый калий, без доступа воздуха или кислорода. [23]
В феномене агглютинации эритроцитов более сильный эффект проявляют металлы высшей валентности. Так, при средней валентности катионов 1 6 эффективная концентрация равняется 100 - 500 микромолей, а при значении средней валентности, равной 3, только 0 1 - 1 0 микромоля. Объяснение этого явления Jandl и Simmons ( 1957) видят в большей активности последних металлов по отношению к функциональным группам оболочки эритроцитов или в большей способности этих металлов проникать через клеточные мембраны тех же эритроцитов. Известно, например, сродство шестивалентного хрома к эритроцитам и проникание именно этой формы хрома через их оболочку, а также его способ - ность связываться с гемоглобином, в меньшей степени с глю-татионом; при этом высокие концентрации вызывают гемолиз. Этот эффект полностью отсутствует при воздействии трехвалентного хрома даже в значительно более высоких концентрациях. [24]
В феномене агглютинации эритроцитов более сильный зф фект проявляют металлы высшей валентности. Так, при средней валентности катионов 1 6 эффективная концентрация равняется 100 - 500 микромолей, а при значении средней валентности, равной 3, только 0 1 - 1 0 микромоля. Объяснение этого явления Jandl и Simmons ( 1957) видят в большей активности последних металлов по отношению к функциональным группам оболочки эритроцитов или в большей способности этих металлов проникать через клеточные мембраны тех же эритроцитов. Известно, например, сродство шестивалентного хрома к эритроцитам и проникание именно этой формы хрома через их оболочку, а также его способ ность связываться с гемоглобином, в меньшей степени с глю-татионом; при этом высокие концентрации вызывают гемолиз. Этот эффект полностью отсутствует при воздействии трехвалентного хрома даже в значительно более высоких концентрациях. [25]
Подобно хрому, марганец при низших валентностях образует соединения основного характера, а его соединения с высшей валентностью обладают кислотным характером. В соединениях марганца со средней валентностью основные окислы постепенно переходят к кислотам. [26]
При анодном растворении гафния и циркония в хлоридных и фторидно-хлоридных расплавах средняя валентность растворяющегося металла меняется в зависимости от состава электролита и плотности тока. Ниже 0 1 а / см2 средняя валентность гафния уменьшается с уменьшением плотности тока. [27]
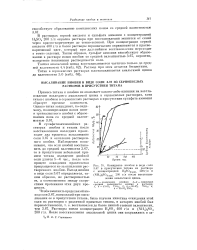 |
Осаждение ниобия в виде соли в присутствии титана из раствора. [28] |
В сульфатноаммонийных растворах ниобия и титана после восстановления последних происходит два процесса: высаливание соли 3.67 и окисление растворенного ниобия. Наблюдения показывают, что если ниобий восстановить до средней валентности 3.67, то в присутствии небольшой примеси титана осаждение двойной соли длится 5 - 6 час. [29]
В результате совместного действия кислорода и углеводорода ионы металла часто находятся в разных валентных состояниях, и в среднем валентность металла соответствует некоторой дробной величине. Так, ион ванадия при окислении нафталина воздухом имеет среднюю валентность - 4 3 вместо 5 в оксиде пятивалентного ванадия. [30]
Страницы: 1 2 3 4
