Средняя валентность
Cтраница 3
Цвет сернокислых растворов ниобия с концентрацией менее 40 % при восстановлении изменяется от синего до темно-зеленого. Синий цвет имеют ионы четырехвалентного ниобия, а темно-зеленый - комплексные ионы со средней валентностью 3.33. Таким образом, в растворах этой концентрации восстановление ниобия на средней валентности 3.67 не задерживается. [31]
Цифры в центре указывают валентность. В тех случаях, когда соединение содержит два или более атомов серы или азота, приводится средняя валентность. [32]
В феномене агглютинации эритроцитов более сильный эффект проявляют металлы высшей валентности. Так, при средней валентности катионов 1 6 эффективная концентрация равняется 100 - 500 микромолей, а при значении средней валентности, равной 3, только 0 1 - 1 0 микромоля. Объяснение этого явления Jandl и Simmons ( 1957) видят в большей активности последних металлов по отношению к функциональным группам оболочки эритроцитов или в большей способности этих металлов проникать через клеточные мембраны тех же эритроцитов. Известно, например, сродство шестивалентного хрома к эритроцитам и проникание именно этой формы хрома через их оболочку, а также его способ - ность связываться с гемоглобином, в меньшей степени с глю-татионом; при этом высокие концентрации вызывают гемолиз. Этот эффект полностью отсутствует при воздействии трехвалентного хрома даже в значительно более высоких концентрациях. [33]
В феномене агглютинации эритроцитов более сильный зф фект проявляют металлы высшей валентности. Так, при средней валентности катионов 1 6 эффективная концентрация равняется 100 - 500 микромолей, а при значении средней валентности, равной 3, только 0 1 - 1 0 микромоля. Объяснение этого явления Jandl и Simmons ( 1957) видят в большей активности последних металлов по отношению к функциональным группам оболочки эритроцитов или в большей способности этих металлов проникать через клеточные мембраны тех же эритроцитов. Известно, например, сродство шестивалентного хрома к эритроцитам и проникание именно этой формы хрома через их оболочку, а также его способ ность связываться с гемоглобином, в меньшей степени с глю-татионом; при этом высокие концентрации вызывают гемолиз. Этот эффект полностью отсутствует при воздействии трехвалентного хрома даже в значительно более высоких концентрациях. [34]
Замена части ионов U4 в положении В катионами той же валентности примерно с таким же или меньшим ионным радиусом приводит к появлению новых соединений сложного состава, содержащих четырехвалентный уран. Комбинация других катионов, имеющих валентности 2, 3 и 4, с пяти - и шестивалентным ураном ведет к понижению средней валентности катиона В и появлению соединений типа перовскита, содержащих Ва2 или Sr2 в положении А и U5 или U6 в положении В решетки. [35]
В результате исследования различных химических соединений ниобия и тантала были предложены методы разделения этих элементов, основанные на осаждении или кристаллизации солей. Голайберсач и Юнг предложили метод очистки ниобия от примесей тантала, основанный на кристаллизации двойного сульфата аммония с сульфатом ниобия, имеющего среднюю валентность ниобия 3.67. Автором и М. И. Андреевой предложен метод очистки ниобия от примеси тантала, основанный на кристаллизации двойного сульфата NII4NbO ( S04) 2 - Вернетом разработан способ разделения титана, ниобия и тантала в солянокислой среде, основанный на различной растворимости двойных хлоридов с хлористым аммонием. [36]
Цвет сернокислых растворов ниобия с концентрацией менее 40 % при восстановлении изменяется от синего до темно-зеленого. Синий цвет имеют ионы четырехвалентного ниобия, а темно-зеленый - комплексные ионы со средней валентностью 3.33. Таким образом, в растворах этой концентрации восстановление ниобия на средней валентности 3.67 не задерживается. [37]
Первая из этих проблем может быть решена по нескольким каналам. Во-первых, температура во внутреннем объеме расплава в металлодиэлектрическом реакторе без всяких затруднений может быть повышена до 2000 - 2400 С; во-вторых, первая стадия процесса может быть оптимизирована таким образом, что средняя валентность урана в его фторидах, достигающих поверхности расплава, будет ниже трех, так что скорость диспропорционирования фторидов урана радикального типа с учетом температуры в жидкой фазе ( - 2000 С) может быть на порядки величины выше; в-третьих, диспропорционирова-ние - это лишь один из каналов восстановления урана; восстановление происходит в среде водорода, причем не только на поверхности; в-четвертых, в данных условиях процесс восстановления урана - это сильно неравновесный процесс: равновесие смещается, поскольку выделяющийся по любому каналу уран будет немедленно тонуть в расплаве из-за своей более высокой плотности. [38]
Первая из этих проблем может быть решена по нескольким каналам. Во-первых, температура во внутреннем объеме расплава в металлодиэлектрическом реакторе без всяких затруднений может быть повышена до 2000 -: - 2400 С; во-вторых, первая стадия процесса может быть оптимизирована таким образом, что средняя валентность урана в его фторидах, достигающих поверхности расплава, будет ниже трех, так что скорость диспропорционирования фторидов урана радикального типа с учетом температуры в жидкой фазе ( - 2000 С) может быть на порядки величины выше; в-третьих, диспропорционирова-ние - это лишь один из каналов восстановления урана; восстановление происходит в среде водорода, причем не только на поверхности; в-четвертых, в данных условиях процесс восстановления урана - это сильно неравновесный процесс: равновесие смещается, поскольку выделяющийся по любому каналу уран будет немедленно тонуть в расплаве из-за своей более высокой плотности. [39]
 |
Молекулярный состав пара некоторых простых веществ. [40] |
В [12], [15], [28] было указано, что периодические изменения атомного номера связаны с закономерным изменением числа холостых электронов, что в свою очередь должно быть связано с симбатным ходом энергий сублимации простых веществ с образованием атомного пара и со средней валентностью тех же элементов по хлору и фтору. [41]
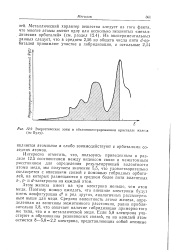 |
Энергетические зоны в объемноцентрированном кристалле железа ( по Буду. [42] |
Атом железа имеет на три электрона меньше, чем атом меди. Средняя валентность атома железа, определенная из величины межатомного расстояния, равна приблизительно 5 8, что означает наличие гибридизации примерно того же типа, что и в металлической меди. [43]
Этими авторами также получены при электролитическом восстановлении раствора красно-коричневого сульфата в 41 % - и серной кислоте темно-зеленые гексагональные дихроидные кристаллы, пропускающие зеленый свет вдоль главной оптической оси и красный через боковые грани. В чистом виде кристаллы не выделены. Титрованием марганцовокислым калием установлена средняя валентность ниобия в этом сульфате в пределах 3.37 - 3.39. Авторы приписывают этому соединению среднюю валентность 3.33, что отвечает вхождению в молекулу пяти атомов ниобия в трехвалентном состоянии и одного пятивалентного атома. [44]
 |
Осаждение ниобия в виде соли в присутствии титана из раствора. [45] |
Страницы: 1 2 3 4