Принцип - подвижное равновесие
Cтраница 3
 |
Влияние концентрации закиси марганца во флюсах с постоянной основно. [31] |
Последнее обстоятельство, по-видимому, связано с увеличением окисленности сварочной ванны с повышением содержания МпО в составе флюса, которая препят - ствует растворению водорода в металле на основании принципа подвижного равновесия. [32]
Если в буферную систему ввести некоторое количество щелочи, например NaOH, то ионы ОН - соединяются с ионами Н с образованием плохо диссоциированных молекул воды, и согласно принципу подвижного равновесия диссоциация уксусной кислоты сдвигается вправо, пополняя количество ионов водорода. Таким образом, при добавлении в буферную систему некоторого количества щелочи общая кислотность уменьшается, а активная остается практически прежней. [33]
Они включают как реакции синтеза, так и распада, подчеркивая тем самым, что эволюция в природе идет в обоих направлениях. Это отвечает принципу подвижного равновесия процессов усложнения и упрощения материальных частиц. [34]
Растворимость газов зависит от температуры. В соответствии в принципом подвижного равновесия ( § 30) в этом случае должно смещаться равновесие в сторону уменьшения растворимости. [35]
Поэтому в соответствии с принципом подвижного равновесия Ле-Шателье растворимость газов уменьшается с нагреванием и увеличивается при охлаждении. [36]
Законы сохранения стационарной ciiMMCTdHH ( 18) можно распространить, как видим, и на квазиизолированные физические системы, проявляющие тенденцию компенсировать диссиметризацию па одном уровне структуры симметризацией на другом. Известный консерватизм вещества по отношению к изменению состояния, описываемый принципом подвижного равновесия Ле-ТПа-телье, заставляет физическую систему оказывать сопротивление и вынужденному изменению ее симметрии. [37]
В заключение вновь подчеркнем следующее. Соответствующие графики, например рис. 11.30 или построенные в масштабе рис. 11.27, б и 11.29, дают возможность довести сначала качественный ( правило фаз), затем полуколичественный ( принцип подвижного равновесия) анализ до количественного результата. Таким образом создается логическая цепочка: что. [38]
В заключение вновь подчеркнем следующее. Соответствующие графики, например рис. 11.30 или построенные в масштабе, рис. 11.27, б и 11.29, дают возможность довести сначала качественный ( правило фаз), затем полуколичественный ( принцип подвижного равновесия) анализ до количественного результата. Таким образом создается логическая цепочка: что. [39]
Ты хорошо знаешь сущность динамического равновесия, - заговорила Адсорбция. Конечно, рассчитываешь использовать его против меня, чтобы освобождать частицы, задержанные на поверхности адсорбента. А принцип подвижного равновесия, принцип, который обычно люди связывают с именами Ле Ша-телье и Брауна, гласит: Если на систему, находящуюся в динамическом равновесии, производится внешнее воздействие, то оно будет благоприятствовать протеканию той из двух противоположных реакций, которая ослабляет это внешнее воздействие. Представь себе, что идет процесс, при котором выделяется какое-то количество тепла, а мы начнем нагревать эту реагирующую смесь. Если система равновесна, она должна противостоять внешнему воздействию. Теплота, внесенная извне, должна использоваться. [40]
Наличие окислов железа в составе флюса-шлака делает маловосприимчивыми швы, выполненные под таким флюсом к содержащейся в нем влаге или ржавчине на поверхности свариваемых кромок. Присутствие FeO на границе межфазной поверхности шлак - металл способствует повышению окислительных условий в сварочной ванне, а это препятствует растворению водорода в жидком металле, образующегося при диссоциации водяного пара. На основании принципа подвижного равновесия увеличение концентрации закиси железа в жидком металле должно способствовать протеканию реакции справа налево. В связи с этим швы, выполненные под флюсами АН-17, АН-17М и АН-43, в меньшей степени склонны к образованию пор по сравнению с идентичными составами флюсов, но без окислов железа. [41]
 |
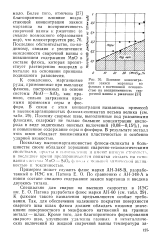
Зависимость растворимости газов в воде от температуры. [42] |
Растворимость газов зависит от температуры. Растворение газов в жидкостях, за небольшим исключением, сопровождается выделением тепла. Тогда, согласно принципу подвижного равновесия ( § 53), при повышении температуры должно происходить смещение равновесия в сторону уменьшения растворимости. [43]
 |
Зависимость растворимости газов в воде от температуры. [44] |
Растворимость газов зависит от температуры. Растворение газов в жидкостях, за небольшим исключением, сопровождается выделением тепла. Тогда, согласно принципу подвижного равновесия ( § 55), при повышении температуры должно происходить смещение равновесия в сторону уменьшения растворимости. [45]
Страницы: 1 2 3 4