Принцип - плотнейшая упаковка
Cтраница 3
Если вспомнить, что в плотнейшей шаровой упаковке шарами заполнено 74 05 %, то станет ясным, что принцип плотнейшей упаковки для молекулярных кристаллов, в общем, оправдывается. [31]
Это относится, например, ко многим силикатам ( слоистым или каркасным), комплексным соединениям и др. Применение принципа плотнейшей упаковки шаров ( ионов) носит тем более искусственный характер, чем сильнее выражена гомеополярность связей между ато-мами. Принцип упаковки молекул выполняется тем хуже, чем больше ослабляется связь между атомами внутри молекулы и чем больше усиливается - между молекулами. [32]
Наиболее общими кристаллохимическими идеями, используемыми в процессе структурного исследования, являются взаимно обусловленные друг другом принцип постоянства атомных, ионных и межмолекулярных радиусов и принцип плотнейшей упаковки атомов, ионов или молекул. [33]
Возможен и другой предельный случай, когда в структурах соединений металлов с неметаллами атомы неметалла небольших размеров занимают пустоты между атомами металла, расположенными по принципу плотнейшей упаковки. У боридов важной особенностью многих структур является наличие связей В-В; по составу и строению бориды обычно сильно отличаются от карбидов и нитридов. Строение карбидов МС2 было описано в гл. Несмотря на то что эти структуры можно рассматривать и как КПУ атомов металла с ионами С22 - в октаэдрических пустотах, все же имеется существенное отклонение от кубической симметрии благодаря крупному размеру и несферической форме ионов С22 -, так что эти карбиды не относят к соединениям внедрения. Совместно с карбидами и нитридами со структурой фаз внедрения иногда рассматривают некоторые оксиды, о которых будет сказано ниже. Поскольку карбиды и нитриды железа намного активнее химически, чем другие описанные здесь соединения, и отличаются от них строением, удобно рассматривать их отдельно. [34]
Их энергия ( 6 - 10 ккал / моль) выше энергии ван-дер-ваальсо-вого взаимодействия ( 1 - 2 ккал / моль), поэтому в кристаллах сначала выполняется принцип насыщения водородных связей, затем осуществляются принципы плотнейшей упаковки. [35]
 |
Координационные числа некоторых катионов в кислородных соединениях. [36] |
В табл. 4 приведены значения радиусов ионов - катионов и анионов, в табл. 5 - координационные числа ряда катионов, обычно осуществляемые в кислородных соединениях - в наиболее широком классе соединений, к которому применимы принципы плотнейшей упаковки. [37]
В пустотах между шарами плотнейших упаковок металлов могут располагаться Si, С, О, Н, N, образуя силициды, карбиды, окислы, гидриды, нитриды. Принцип плотнейшей упаковки остается справедливым и для ионных соединений: анионы образуют плотнейшую упаковку, а катионы размещаются в пустотах. [38]
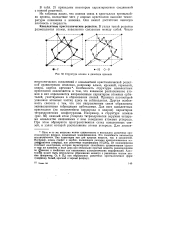 |
Структура алмаза и диоксида кремния. [39] |
Особенность структуры ковалентных кристаллов заключается в том, что взаимное расположение атомов в них определяется направленным характером атомных орби-талей, участвующих в образовании связей. Принцип плотнейшей упаковки атомных частиц здесь не соблюдается. Другая особенность связана с тем, что эти направленные связи образованы эквивалентными гибридными орбиталями. Для всех ковалентных кристаллов ( за исключением кислорода в кварце) характерна тетраэдрическая конфигурация. Например, в структуре алмаза ( рис. 50) каждый атом углерода тетраэдрически окружен четырьмя ковалентно связанными с ним соседними атомами углерода. При этом образуется пространственная сетка ковалентных связей, в узлах которой расположены атомы углерода. [40]
Кристаллы комплексных соединений занимают промежуточное положение между ионными и молекулярными, поскольку здесь связи имеют частично ковалентный, частично ионный характер, а иногда наряду с этими двумя типами связи встречаются и связи ван-дер-ваальсовского типа. Поэтому ни принцип плотнейшей упаковки шаровых ионов, ни концепция плотнейшей упаковки жестких группировок атомов не осуществляется в комплексных кристаллах в полной мере. Пользоваться этими представлениями приходится с большой осторожностью. [41]
 |
Зависимость остаточного напряжения сдвига Р, интенсивности ИК-спектров поглощения и показателя преломления п р грозненского парафина от температуры t. [42] |
В низкотемпературной фазе молекулы располагаются по принципу плотнейшей упаковки, когда выступы одних молекул входят во впадины других, что обеспечивает системе высокую прочность и, следовательно, высокие значения физико-механических показателей. [43]
 |
Решетка рутила ТЮ2.| Решетка [ IMAGE ] Решетка. [44] |
Раньше предполагали, что причиной упорядоченного размещения частиц в кристаллах является анизотропность самих атомов: думали, что взаимодействие между атомами в сильной мере зависит от взаимной ориентации атомов. Однако оказалось, что главная причина упорядоченного размещения частиц в кристаллах более проста - это принцип плотнейшей упаковки. Вследствие взаимного притяжения частицы стремятся разместиться возможно ближе друг к другу, но при чрезмерном сближении проявляются силы отталкивания, вследствие чего каждая частица может быть уподоблена как бы непроницаемому шарику определенного радиуса. При плотнейшей упаковке шаров 26 % объема приходится на пустоты между шарами. [45]
Страницы: 1 2 3 4 5