Природа - анион
Cтраница 2
 |
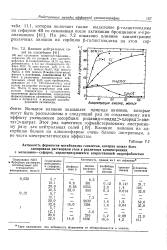
Влияние природы аниона солей галогенводо-родных кислот на скорость коррозии железоуглеродистых сплавов. [16] |
Влияние природы аниона на скорость коррозии железоуглеродистых сплавов показано на рис. 19, из которого видно, что наибольшую коррозионную активность имеют анионы фтора и хлора. [17]
Влияние природы аниона на строение двойного электрического слоя проявляется при положительном заряде поверхности и в области потенциалов, соответствующих небольшим отрицательным значениям плотности заряда на электроде. При сильной катодной поляризации кривые емкости на всех исследованных металлах сливаются, что указывает на десорбцию поверхностно-активных анионов с поверхности электрода. В этой области потенциалов некоторую информацию о структуре двойного электрического слоя дает исследование влияния природы катиона на С - ф-кривые. [18]
Изменение природы аниона в солях АН 1ЛпГзп вызывает хотя и и небольшие, но вполне отчетливые изменения положения полосы поглощения СН2 - гругшы. [20]
Следовательно, природа аниона является решающей при определении растворимости, образовании ионных пар и гомосопря-жении солей в ацетонитриле. Так, растворимость хлорида натрия составляет лишь З - Ю 5 моль / л при 25 С; едкий натр также очень мало растворим. Наоборот, соли с крупными или хорошо поляризуемыми одновалентными анионами обычно имеют более высокую растворимость. Например, иодиды, перхлораты и пикраты растворяются умеренно, так же как галиды тетраалкиламмония. Так как ацетонитрил также и плохой донор протонов, коэффициент активности переноса водородных ионов тоже высокий. [21]
 |
Установка для получения аммиака. [22] |
Как влияет природа аниона на характер термического разложения солей аммония. [23]
Рассмотрено влияние природы аниона и катиона на процесс электровыделения. Для этого в различные соли, отличающиеся катионом ( К, Na, Li) или анионом ( NO3 -, C1 -, СО3 - 2, SO4 - 2, CHCOO -, РО4 - 3), вводили одинаковые количества ( Ы0 - 4 % в расчете на соль) элементов-примесей, после чего электрохимически выделяли примеси в выбранных условиях. [24]
Специфическое влияние природы анионов на кинетику электродных процессов описано во многих работах. Так, например, при добавлении галоид-ионов в раствор ацетата пентаммиаката трехвалентного кобальта на полярограммах появляется кинетическая предволна, высота которой определяется скоростью вступления галоид-иона во внутреннюю сферу комплекса ( вместо ацетат-аниона), причем, по мнению Влчека и Куты [248], эта реакция резко ускоряется под влиянием поля электрода. Городецкий и Лосев [250] нашли, что галоид-ионы, взаимодействуя с промежуточными продуктами электродного процесса, значительно ускоряют ионизацию висмута из его амальгамы или разряд его ионов из растворов хлорной кислоты. [25]
Выявлено влияние природы поглощаемых анионов и момента окончания процесса поглощения на характер расположения анионов в слое поглотителя. [26]
Исследование влияния природы аниона кислоты-осадителя на устойчивость золей показало ( см. таблицу), что положение максимума устойчивости закономерно изменяется при изменении основных физико-химических характеристик кислоты. Такое смещение положения ИЭТ золей ПКК с изменением среды может быть следствием изменения электронодонорных свойств аниона, хотя не исключена возможность того, что определенное значение имеет также необходимое для достижения одного и того же рН увеличение концентрации кислоты-осадителя по мере уменьшения степени ее ионизации. [27]
Большое влияние оказывает природа анионов, которые могут быть расположены в следующий ряд по создаваемому ими эффекту уменьшения десорбции: роданид иодидхлоридаце-татцитрат. Влияние анионов на адсорбцию белков на алкилсефарозе очень близко лиотропным, а не чисто электростатическим эффектам. [29]
Кр зависит от природы аниона, увеличиваясь в ряду нитратборатсульфаткарбонат. При рН10 и концентрации NH4OH0 5 M кинетика анодного растворения и пассивация практически не зависят от природы аммонийной соли. В щелочных растворах в присутствии аммиака / Кр возрастает, а нарушение пассивного состояния ионами NO3 - и SO42 - затрудняется. Плотность тока пассивации в растворах ( NH4) 2CO3 с ростом рН снижается, и в остальных аммонийных растворах [ NH4NO3; ( NH4) 28 ( 1) 4 ] проходит через минимум ( положение которого зависит от концентрации и природы соли) и максимум. Критический потенциал пассивации в исследованных растворах снижается с ростом рН и практически не зависит от природы и концентрации электролита. [30]
Страницы: 1 2 3 4 5