Природа - катион
Cтраница 1
Природа катиона играет значительную роль не только в процессе адсорбции воды, но и в процессах адсорбции других полярных молекул и молекул с я-связями. Так, было показано [51, 63], что металлзамещеп-ные цеолиты, катионы которых образуют с аммиаком комплексы, характеризуются повышенной активностью к аммиаку. Изотермы сорбции на никель -, цинк -, кобальт - и кадмийзамещенных цеолитах лежат значительно выше изотермы сорбции аммиака на цеолитах в натриевой форме. [1]
Природа катиона и степень его замещения в цеолите играют существенную роль во взаимодействии сорбата с адсорбентом и в его удерживании. Непредельные соединения сильно удерживаются на цеолитах типа X, содержащих серебро. Цеолиты, содержащие серебро и кадмий, селективно удерживают непредельные соединения. [2]
 |
Молекулярные сита типа X с замещенными ионами 16. [3] |
Природа катиона в цеолите оказывает большое влияние на хрома-тографические свойства молекулярных сит и на разделение внутри данного углеродного числа. Этот факт имеет большое значение для аналитической практики. [4]
Природа катионов, улавливаемых из раствора катионитом, сказывается не только на их способности к взаимному вытеснению в процессе катионирования, но и на способности к разделению в слое поглотителя. [5]
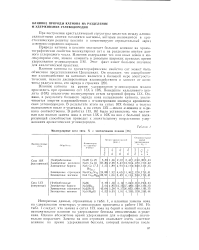
Природа катиона играет значительную роль не только в процессе адсорбции воды, аммиака, углекислого газа, но в процессе адсорбции ненасыщенных углеводородов и молекул с л-связями. Из температурной зависимости удерживаемых объемов индивидуальных газов определены теплоты адсорбции предельных и непредельных углеводородов, а также окиси углерода. Из табл. 22 следует, что теплоты адсорбции цеолитами зависят от природы индивидуального газа. Для одного и того же предельного углеводорода теплота адсорбции практически мало зависит от ион-металла цеолита. При увеличении в углеводороде числа углеродных атомов теплота адсорбции возрастает на 2 - 3 ккал / моль на одну СН2 - группу. [6]
 |
Молекулярные сига типа X с замещенными ионами 16. [7] |
Природа катиона в цеолите оказывает большое влияние на хрома-тографические свойства молекулярных сит и на разделение внутри данного углеродного числа. Этот факт имеет большое значение для аналитической практики. [8]
Природа катиона играет незначительную роль, но комплексные анионы, содержащие металлы, обычно проявляют большее стремление к выходу на поверхность и дают больший отрицательный заряд, чем простые анионы. [9]
Природа катионов оказывает незначительное влияние. Однако ионы сложного строения, содержащие металлы, обнаруживают большую склонность накапливаться у поверхности раствора, чем простые ионы; очевидно, в подобных случаях отрицательный заряд слоя будет больше. [10]
Природа катионов устанавливается по потенциалам полуволны, а их концентрация - по высотам соответствующих волн. [11]
Природа катионов и металл-кислородные ( М - О) колебания в их аквакомплексах. [12]
Природа катиона проявляется в трех факторах: величине заряда катиона, его радиусе и его электронной конфигурации. [13]
Природа катиона ( Na, К), не сказываясь на структуре гидроксокомплексов А1 ( Ш), влияет на их концентрацию - в натриевых системах концентрация полимерных образований выше. При концентрациях растворов выше 100 г / л начинают сказываться катион-анионные взаимодействия, что и влияет на концентрацию полимерных анионных образований. [14]
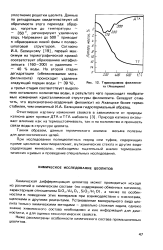 |
Термограмма филлипси-та ( Ахалцихе. [15] |
Страницы: 1 2 3 4 5