Природа - кислота
Cтраница 1
Природа кислот, разделенных таким образом, определяется по коэфициентам обмыливания. Нельзя сказать, однако, что подобное определение всегда возможно. [1]
Природа кислоты не установлена за неимением достаточного количества материала. [2]
Природа кислот, содержащих As в состоянии низшей степени окисления, не твердо установлена, и они скорее считаются гидрзтированными окислами As. Однако в солях арсенит-анион известен как в виде орто-арсенита, так и в виде более сложных форм. [3]
 |
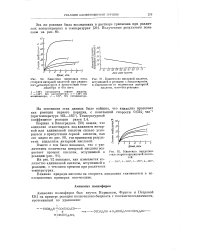
Влияние концентрации водного диоксана.| Константы скорости реакции протодемеркурирования C6HBHgBr. [4] |
Природа кислоты оказывает значительное влияние на ход протолиза. Показано, что катализ связан не с ионами Н или С1 -, а с молекулами НС1 в виде ионных пар. Монохлоруксусная, фосфорная и трихлоруксусная кислоты в водном диоксане, содержащем от 10 до 35 % воды, дают кинетику первого порядка с весьма близкими величинами klt причем для трихлоруксусной кислотного катализа не наблюдается. Зависимость скорости реакции от содержания воды в диоксане сложна и неодинакова для разных кислот. [5]
Природа кислот, содержащих As в состоянии низшей степени окисления, не твердо установлена, и они скорее считаются гидратированными окислами As. Однако в солях арсенит-анион известен как в виде орто-арсенита, так и в виде более сложных форм. [6]
Природа кислоты не установлена за неимением достаточного количества материала. [7]
Природа кислот и оснований всегда интересовала исследователей, а в последнее время интерес к ним особенно возрос в связи с тем, что бурное развитие химии дало обилие нового экспериментального материала, который настоятельно требует широких теоретических обобщений, охватывающих все многообразие кислотно-основных взаимодействий. [8]
Двухосновная природа кислоты была установлена путем титрования. [9]
 |
Количество янтарной кислоты.| Кинетика ацидолиза зтилстоарата адипиновой кисло. [10] |
Влияние природы кислоты на скорость ацидолиза следованных примерах неотчетливо. [11]
В природе кислоты весьма распространены, и значение их в народном хозяйстве огромно. [12]
В природе кислоты встречаются очень часто в свободном виде и в форме сложных эфиров. Еще недавно преобладало мнение о том, что кислоты выше С1 (, с нечетным числом углеродных атомов в молекуле не встречаются в природе. Газовую хроматографию впервые применили именно для разделе ния органических кислот. [13]
В природе кислоты ряда бензола встречаются главным образом в виде сложных эфиров, содержащихся в растительных смолах. [14]
Исследование влияния природы кислоты на обменную емкость 7-оксида алюминия показало, что ионный обмен сопровождается нейтрализацией гидроксильных групп на поверхности оксида алюминия. [15]
Страницы: 1 2 3 4