Природа - галоид
Cтраница 2
Зависимость плавкости и летучести галогенидов от природы галоида проявляется различно. При наличии ионных структур температуры плавления и кипения по ряду F - С1 - Вг - I обычно понижаются, при наличии молекулярных структур - повышаются. [16]
Скорость этой обменной реакции зависит как от природы галоида в галоидоводородных кислотах, так и от строения спирта. [17]
Электронная плотность на атоме металла зависит от природы галоида и растет в ряду I, Вч С1, причем в случае никеля эта тенденция выражена значительно сильнее, чем для палладия. [18]
Зависимость полярности связи Э - Г от природы галоида. [19]
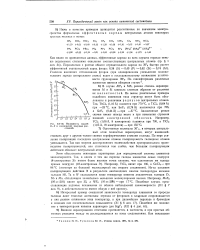 |
Полярность связей Э - F и сокращение ядерных расстояний. [20] |
Интересный пример смешанной зависимости температур плавления от природы галоида дают тяжелые лантаниды: переход от фторидов к хлоридам сопровождается у них резким снижением этих температур, а при дальнейшем переходе к бромидам и иодидам они последовательно повышаются ( XI § 6 доп. Подобное же положение с температурами кипения характерно для HgF2 ( XII § 4 доп. [21]
Легкость отщепления галоида от углеводородного радикала зависит от природы галоида и строения радикала. Иод легче отщепляется, чем бром, а этот последний - легче, чем хлор. Так, хлористый винил СН2 СН-С1 практически не гидролизуется водой, даже в присутствии щелочей. [22]
Как и при других синтезах с магнинорганическими соединениями, природа галоида оказывает значительное влияние па ход реакции и на выход продукта. Удовлетворительные результаты обычно получаются лишь с бромпроизводными. Иодпроиз-водные реагируют энергичнее бромистых соединений, однако в этом случае получение реактива Иоцича часто сопровождается побочными реакциями. Общеизвестно, что применение иод-произзодных при гриньяровских синтезах способствует реакции Вюрца. Наряду с этим иодпроизводпые часто оказывают восстанавливающее действие. При получении третичных ацетиленовых спиртов, отличающихся склонностью к дегидратации, применение иодпроизводных может привести к дегидратации карбинола. Нередко подобная дегидратация под влиянием иодпроизводных сопровождается взрывоподобной полимеризацией и разложением продуктов реакции. [23]
Столь резкое различие в течении реакции в зависимости от природы галоида не замечено при многочисленных реакциях обменного разложения различных галоидпроизводных классической органической химии и потому несомненно представляют большой интерес. Попытки привлечения к пониманию вновь изученных нами реакций электронных представлений были неудовлетворительны. [24]
На примере синтеза ди-н-бутилртути изучена [17] зависимость выхода диалкилртути от природы галоида в галоидном алкиле и процентного содержания амальгамы. [25]
При реакции галоидзамещенных простых эфиров с литийорганическими соединениями в зависимости от природы галоида и от его положения по отношению к эфирной группе возможны разные направления реакции: конденсация, отщепление НХ, обмен галоида на литий. Чем дальше от эфирной связи стоит галоид, тем более склонны галоиди-рованные эфиры к конденсации. Исходя из у-хлор -, у-бром. [26]
Реакционноспособность галоида в органических соединениях зависит от целого ряда факторов: от природы галоида, от характера соседних групп и от типа связи его с углеродом, к которому присоединен галоид, и природы остальной части молекулы. Последний из этих факторов имеет большое значение. В табл. 32 показано влияние удлинения цепи на относительную реакционноспособность галоида в галоидных алкилах. Приведенная количественная характеристика подвижности галоида выведена на основании изучения скорости реакции галоидных алки-лов с различными веществами. [27]
Характер взаимодействия зависит от строения радикала фосфористой кислоты, строения галоидпроизводного, природы галоида и условий проведения реакции. В эфирном растворе бромистый трифенилметил, хлористый и бромистый трис - ( п-толил) - метилы образуют с диэтилфосфористым и диизобутилфосфори-стым натрием эфиры триарилметилфосфоновых кислот. [28]
Характер взаимодействия зависит от строения радикала фосфористой кислоты, строения галоидпроизводного, природы галоида и условий проведения реакции. В эфирном растворе бромистый трифенилметил, хлористый и бромистый трис - ( га-толил) - метилы образуют с диэтилфосфористым и диизобутилфосфори-стым натрием эфиры триарилметилфосфоновых кислот. [29]
Реакционноспособность галоида в органических соединениях зависит от целого ряда факторов: от природы галоида, от характера соседних групп и от типа связи его с углеродом, к которому присоединен галоид, и природы остальной части молекулы. Последний из этих факторов имеет большое значение. В табл. 32 показано влияние удлинения цепи на относительную реакционноспособность галоида в галоидных алкилах. Приведенная количественная характеристика подвижности галоида выведена на основании изучения скорости реакции галоидных алки-лов с различными веществами. [30]
Страницы: 1 2 3 4