Природа - полярная группа
Cтраница 1
Природа полярной группы и противоионов ( внутри классов анионных и катионных ПАВ) слабо влияют на со-любилизацию. Однако при переходе от анионактивных к ка-тионактивным ПАВ при одинаковом углеводородном радикале наблюдается заметное повышение солюбилизирующей способности. [1]
Хотя влияние природы полярных групп на обменное равновесие заметно проявляется только в равновесных системах, в которых участвует ион водорода, можно отметить и другие случаи обменного равновесия, при котором также сказывается влияние природы полярных групп. Это явление может быть объяснено различно. Во-первых, коэффициенты активности карбоксильных солей щелочноземельных металлов могут быть несколько меньше, чем соответствующих сульфокислых солей. Во-вторых, растворимость карбоксильных солей может быть меньше, чем сульфокислых. В-третьих, катионы щелочноземельных металлов могут образовать с карбоксильными группами слабо диссоциированные комплексы. Любой из этих трех причин можно объяснить различие в свойствах карбоксильных и сульфокислотных смол. [2]
Хотя влияние природы полярных групп на обменное равновесие заметно проявляется только в равновесных системах, в которых участвует ион водорода, можно отметить и другие случаи обменного равновесия, при котором также сказывается влияние природы полярных групп. Это явление может быть объяснено различно. Во-первых, коэффи -, циенты активности карбоксильных солей щелочноземельных металлов могут быть несколько меньше, чем соответствующих суль-фокислых солей. Во-вторых, растворимость карбоксильных солей может быть меньше, чем сульфокислых. В-третьих, катионы щелочноземельных металлов могут образовать с карбоксильными группами слабо диссоциированные комплексы. Любой из этих трех причин можно объяснить различие в свойствах карбоксильных и сульфокислотных смол. [3]
В зависимости от природы полярной группы принято различать ионогенные и неионогенные ПАВ. В свою очередь ионогенные ПАВ подразделяются на катионо - и анионоактивные в зависимости от знака поверхностно-активного иона. Анионоактивные ПАВ являются эффективными стабилизаторами прямых ( масло / вода), а катионоактивные - обратных ( вода / масло) эмульсий. [4]
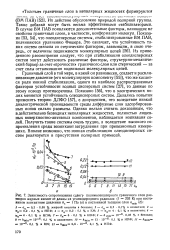
Их действие обусловлено природой полярной группы. Такие добавки могут быть весьма эффективными стабилизаторами. В случае ВМ ПАВ появляются дополнительные факторы, влияющие нг свойства граничных слоев, в частности, конформация молекул. Показано [53, 54], что олеодисперсные системы, стабилизированные ВМ ПАВ, подчиняются уравнению Фишера. Из приведенного рассмотрения следует, что при стабилизации олеодисперсных систем могут действовать различные факторы, структурно-механический барьер за счет прочности граничного слоя или стерический - за счет силы отталкивания подвижных молекулярных цепей. Граничный слой в той мере, в какой он равновесен, создает и расклинивающее давление ( его молекулярную компоненту [55]), что же касается роли ионной стабилизации, одного из наиболее распространенных факторов устойчивости водных дисперсных систем [27], то данные по этому поводу противоречивы. Показано [56], что в электрических полях меняется устойчивость олеодисперсных систем. Делались попытки применить теорию ДЛФО [57], с допущением, что вследствие низкой диэлектрической проницаемости среды диффузные слои адсорбированных ионов сильно размыты. Однако нельзя считать доказанным, что в действительно безводных неполярных жидкостях, полностью лишенных поверхностно-активных компонентов, наблюдается ионизация солей. Получить такие системы очень трудно, а вследствие высокого сопротивления среды возникают затруднения при прецезионных измерениях. Вполне возможно, что ионная стабилизация олеодисперсных систем реализуется в присутствии полярных примесей. [6]
Как влияет на ККМ природа полярной группы молекул ПАВ. [7]
Wo - константа, зависящая от природы полярной группы. [8]
Независимость же этой величины и от природы полярной группы свидетельствует о том, что она определяется сечением углеводородной цепи. [9]
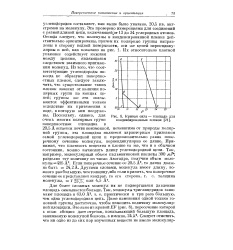 |
Кривая сила - площадь для конденсированных пленок. [10] |
А остается почти неизменной, независимо от природы полярной группы, эта площадка является характерным признаком самой углеводородной цепи и предположительно равна поперечному сечению молекулы, перпендикулярно ее длине. [11]
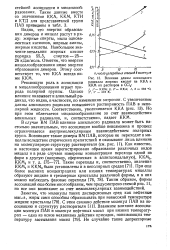 |
Влияние длины алкильного радикала жирных кислот на ККА и ККМ их растворов в СС14. [12] |
Решающую роль в ассоциации и мицеллообразовании играет природа полярной группы. Однако влияние оказывает и алкильный радикал, что видно, в частности, по изменениям энтропии. С увеличением длины алкильного радикала повышается растворимость ПАВ в неполярной жидкости. Но при этом облегчается мицеллообразование за счет взаимодействия алкильных радикалов, и, соответственно, падает ККМ. [13]
Вязкость длинноцепочечных алифатических соединений весьма чувствительна к природе полярных групп. У жирных кислот вязкость обычно меньше, чем у соответствующих спиртов и тем более аминов. Важное значение имеет рН подложки. [14]
В каких случаях величина поверхностной активности зависит: от природы полярной группы молекулы ПАВ; от природы и размеров неполярной ( гидрофобной) части молекулы ПАВ. [15]
Страницы: 1 2 3 4