Viiia-группа
Cтраница 1
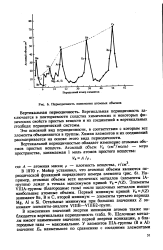 |
Периодичность изменения атомных объемов. [1] |
Элементы VIIIA-группы ( благородные газы) после щелочных металлов имеют наибольшие атомные объемы. Первый минимум кривой Vk / ( Z) занимают Be, В и С, второй минимум - элементы третьего периода Mg, A1 и Si. Остальные минимумы при больших значениях Z занимают элементы-аналоги VIIIB - УП1Б2 - групп. [2]
Особое место среди простых веществ VIIIA-группы занимает гелий. Во-первых, это наиболее трудно сжижаемый газ; во-вторых, это единственный элемент, для которого твердое состояние достигается только при повышенном давлении ( около 25 - Ю6 Па), в-третьих, в жидком состоянии гелий обладает особыми свойствами. Эта жидкость с особыми и уникальными свойствами: она практически не обладает вязкостью ( сверхтекучесть), имеет колоссальную теплопроводность ( в 3 - 108 раз больше гелия-I), а также проявляет ряд других аномальных эффектов. Поэтому сверхтекучий Не - П называют квантовой жидкостью. [3]
В силу химической инертности элементы VIIIA-группы в природе встречаются только в свободном состоянии главным образом в атмосфере. [4]
Особое место среди простых веществ VIIIA-группы занимает гелий. Во-первых, это наиболее трудно сжижаемый газ; во-вторых, это единственный элемент, для которого твердое состояние достигается только при повышенном давлении; в-третьих, в жидком состоянии гелий обладает особыми свойствами. Эта жидкость с особыми и уникальными свойствами: она практически не обладает вязкостью ( сверхтекучесть), имеет колоссальную теплопроводность ( в 3 - Ю8 раз больше гелия-1), а также проявляет ряд других аномальных эффектов. Эти явления связаны с тем, что при температуре 1 - 2 К длина волны де Бройля для атома гелия сравнима со средним межатомным расстоянием. Поэтому сверхтекучий Не - П называют квантовой жидкостью. [5]
Особое место среди простых веществ VIIIA-группы занимает гелий. Во-первых, это наиболее трудно сжижаемый газ; во-вторых, это единственный элемент, для которого твердое состояние достигается только при повышенном давлении; в-третьих, в жидком состоянии гелий обладает особыми свойствами. При отмеченной температуре наблюдается так называемый фазовый переход II рода ( не сопровождаемый тепловым эффектом) и вплоть до сколь угодно низких температур, приближающихся к абсолютному нулю; гелий существует в виде жидкого Не-И. Эта жидкость с особыми и уникальными свойствами: она практически не обладает вязкостью ( сверхтекучесть), имеет колоссальную теплопроводность ( в 3 - Ю8 раз больше гелия-1), а также проявляет ряд других аномальных эффектов. Эти явления связаны с тем, что при температуре 1 - 2 К длина волны де Бройля для атома гелия сравнима со средним межатомным расстоянием. Поэтому сверхтекучий Не - П называют квантовой жидкостью. [6]
Затем были открыты все остальные элементы VIIIA-группы - благородные газы. [7]
Сквозная полная аналогия не просматривается и среди элементов VIIIA-группы, хотя все они относятся к благородным газам. Однако и здесь можно выделить типические элементы ( неон и аргон) и элементы подгруппы криптона, у которых в отличие от типических присутствует заполненная предвнешняя ( п - 1) 10-оболочка. Следовательно, и в этой группе, как и у всех р-элементов, существует неполная электронная аналогия между типическими элементами и остальными / 7-элементами VIII группы. Следует отметить, что здесь типические элементы вообще не определяют облик группы в целом в силу своей химической инертности. [8]
Из рассмотрения электронных конфигураций атомов видно, что элементы VIIIA-группы ( Не, Ne, Ar и др.) имеют завершенные s - и / - подуровни одновременно ( s2p6), такие конфигурации обладают высокой устойчивостью и обеспечивают химическую пассивность, благородных газов. Незавершенные подуровни и электроны на них иначе называются валентными, так как именно они могут участвовать в образовании химических связей между атомами. [9]
Исходя из справочных значений энергии ионизации и электроотрицательности для элементов VIIIA-группы, объясните принципиальную возможность перехода из нулевого в положительные состояния окисления и участия в химических реакциях - аргона ( ср. [10]
Как следует из приведенных данных, свойства простых веществ элементов VIIIA-группы закономерно изменяются по мере увеличения атомной массы. [11]
В силу большого своеобразия химических свойств выделяют отдельно благородные газы-элементы VIIIA-группы Периодической системы. Исследования последних лет позволяют, тем не менее, причислить некоторые из них ( Кг, Хе, Rn) к неметаллам. [12]
Среди р-элементов встречаются весьма инертные вещества - благородные газы ( элементы VIIIA-группы) с полностью заселенными s - и р - АО ( ns np), не образующие поэтому молекул и существующие в обычных условиях в виде газа, состоящего из атомов. [13]
Комплексообразователями могут быть почти все элементы периодической системы, даже элементы VIIIA-группы. В частности, получен октафтороксенат ( VI) цезия CsztXeFg ] в виде желтых кристаллов, устойчивых при нагревании до 400 С. Реже встречаются комплексные соединения, в которых комплексообразователями являются щелочные и щелочно-земельные элементы. [14]
Приведите все возможные доводы размещения калия в IA-группе, а аргона-в VIIIA-группе, хотя аргон тяжелее калия. [15]
Страницы: 1 2 3