Присоединение - катион
Cтраница 3
 |
Взаимодействие граничных орбиталей в этене и цис-1 3-бутадиене. [31] |
Аналогично было описано присоединение катиона к олефиновой двойной связи как взаимодействие НСМО катиона с ВЗМО ( л) двойной связи. В простых реакциях присоединения этого типа затрагиваются одновременно три атомных центра. В этой главе будут рассмотрены процессы, представляющие собой согласованные реакции с циклическим переходным состоянием. Наиболее известным примером является реакция Дильса-Альдера; одно время ее называли реакцией без механизма, однако Вудвард и Гофман показали, что стереохимию таких реакций можно выяснить, если рассмотреть взаимодействие между граничными орбиталями. Так, на рис. 12.1 изображено взаимодействие этена и бутадиена. [32]
То, что скорость присоединения JC1 меньше, чем скорость присоединения Вг - С1, несмотря на то, что от атома иода легче оттянуть электроны ( с образованием катиона), чем от брома, объясняется следующим образом. Первая стадия реакции - присоединение катиона галогена к молекуле олефина - процесс медленный, так как катион реагирует с нейтральной молекулой. Далеко не всякое соударение катионов с нейтральной молекулой приводит к образованию связи галоген - углерод. Поэтому скорость первой, самой медленной, стадии реакции зависит от химической активности катиона галогена. [33]
То, что скорость присоединения J - С1 меньше, чем скорость присоединения Вг - С1, несмотря на то что от атома йода легче оттянуть электроны ( с образованием катиона), чем от брома, объясняется следующим образом. Первая стадия реакции - присоединение катиона галогена к молекуле олефина - процесс медленный, так как катион реагирует с нейтральной молекулой. Далеко не всякое соударение катиона с нейтральной молекулой приводит к образованию связи галоген-углерод. Поэтому скорость первой, самой медленной, стадии реакции зависит от химической активности катиона галогена. [34]
Эта схема, в сущности, является расширенным приложением схемы Уйнстейна для описания реакций мономолекулярного нуклеофильного замещения SVl-типа у насыщенного атома углерода ( гл. Приведенные выше даные по присоединению катиона RS и сульфенгалогенидов находятся в хорошем соответствии с последовательностью превращений, предполагаемой в данной схеме. [35]
Рост цепи происходит путем присоединения к иону карбония молекулы мономера с поляризованной двойной связью. Обрыв цепи наблюдается при присоединении катиона и особенно протона. По такой схеме протекает анионная полимеризация. [36]
К реакциям [ 4л 2п ] - циклоприсоединения относятся и реакции диенов с ионными реагентами. Так протекает, например, присоединение 2-метил-аллильного катиона к циклопентадиену. [37]
Трудность фиксации аренониевых ионов, имеющих у кольцевого р3 - гибридного атома углерода атом водорода и сильно электроотрицательный заместитель, связана с легкостью отщепления протона, переходящего далее к более основному центру. Значительно устойчивее должны быть ионы, соответствующие присоединению катиона нитрония и других гетероатомных электрофильных частиц к замещенному атому углерода ароматического кольца. [38]
Однако эти связи идентичны только в том случае, когда анионы находятся в изолированном состоянии. Как будет показано в следующем разделе, при присоединении катионов к этим анионам последние несколько поляризуются. В некоторой степени связи РН и PS тоже принимают участие в общем сопряжении связей в анионах ( см. разд. [39]
Реакция Прилежаева относится к числу электрофильных замещений атака НО из НО ( ООССвН5) е, см. стр. Она особенно ясно показывает, насколько труднее протекает реакция присоединения катиона по тройной связи в отличие от двойной. [40]
По существующим в данное время представлениям, образование активных центров при ионной полимеризации в большинстве случаев представляет собой процесс кислотно-основного характера. Начальным актом, в результате которого образуются активные центры, является присоединение катиона или аниона к молекуле мономера. [41]
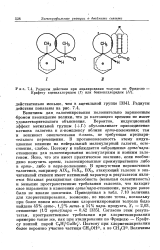 |
Радиусы действия при ацилировании толуола по Фриделю Крафтсу ацетилхлоридом ( / или бензоилхлоридом ( / /. [42] |
Величины для, галогенирования положительно заряженным бромом неожиданно велики, что до настоящего времени не имеет удовлетворительного объяснения. Вероятно, индукционный эффект метальной группы ( I -) обусловливает присоединение катиона галогена к я-комплексу вблизи орто-положения; там и возникает окончательная 0-связь, не требующая предварительного перемещения. [43]
 |
Островные кремнекислородные радикалы. [44] |
Главным элементом структуры широко распространенных в почве кислородных соединений кремния является кремнекислородный тетраэдр ( SiO4) 4 -, в вершинах которого располагаются четыре иона кислорода, а в центре - ион кремния. Кремнекислородный тетраэдр обладает четырьмя свободными валентными связями, которые могут быть компенсированы присоединением катионов или соединением с другими кремнекислородными тетраэдрами. [45]
Страницы: 1 2 3 4