Присоединение - первый электрон
Cтраница 2
В реакциях другого типа участвуют радикалы и ион-радикалы, образовавшиеся в результате присоединения первого электрона. Электролиз на ртутном донном электроде протекает в течение времени, достаточного для превращения бирадикала в 4 - ( 1 -гидроксиэтил) ацетофенон. Превращение бирадикала в кетоспирт происходит в результате кислотно-основного катализа. [16]
Электрохимическая реакция ( 3, е) протекает в две стадии, причем присоединение первого электрона замедленно. [17]
Разряд на катоде двухвалентных ионов меди в сульфатном электролите происходит по стадийному механизму с замедленной стадией присоединения первого электрона в катодном и второго электрона в анодном процессах. На стадийный характер электрохимических реакций оказывают влияние вводимые в электролит добавки, главным образом органической природы. [18]
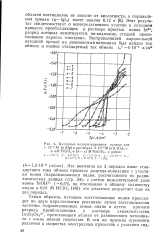 |
Катодные поляризационные кривые для. [19] |
Этот результат свидетельствует о непосредственном участии в катодном процессе преобладающих в растворе простых ионов In3, разряд которых лимитируется, по-видимому, стадией присоединения первого электрона. [20]
Еще одно доказательство этого механизма состоит в том, что пропиоловая кислота НС ССООН не способна восстанавливаться в доступном интервале потенциалов, поэтому декарбоксилирование не может происходить до присоединения первого электрона. [21]
Так, в 1946 г. Б. В. Некрасов [104] при расчете электроотрицательностей ( электросродства, по его терминологии) принял во внимание лишь те потенциалы ионизации, которые характеризуют энергию присоединения первого электрона к законченному слою, например первый Р натрия и седьмой Р фтора. [22]
Следует отметить, что отсутствие двух одноэлектронных волн на полярограммах большинства галоидозамещенных еще не является аргументом в пользу протекания реакции их восстановления по механизму, аналогичному механизму SN - Дело в том, что медленной стадией является стадия присоединения первого электрона ( на скорость которой оказывают влияние все те факторы, которые влияют на скорость радикальных реакций), а присоединение второго электрона к образующимся радикалам совершается столь быстро, что радикалы не успевают вступить ни в какие химические реакции с образованием электрохимически неактивных продуктов. [23]
 |
Порфирин face-to - face почкой из шести атомов. [24] |
Показано [219], что адсорбированный фталоцианин кобальта ускоряет только двухэлектронную реакцию, а в случае фталоциа-нина железа возникает прямая реакция до воды. F, что соответствует замедленности присоединения первого электрона. [25]
Обращают на себя внимание отрицательные величины для О и S: присоединение двух электронов к атомам кислорода или серы требует затраты энергии. Объясняется это тем, что после присоединения первого электрона ( положительное X) второй ими сильно отталкивается; на преодоление этого отталкивания должна быть атрэчена энергия. [26]
Реакция имеет первый порядок по иону гипохлорита. Значение а-0 5 указывает, что медленной стадией является присоединение первого электрона. [27]
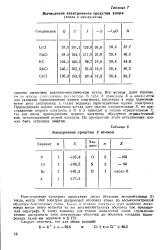 |
Электронное сродство X атомов. [28] |
Все методы дают близкие, но не вполне совпадающие результаты. Присоединение одного электрона всегда дает сильно - д-хтожительные X, но присоединение второго электрона к О и S приводит к сильно отрицательным X, так как после присоединения первого электрона образуется отрицательный коя, отталкивающий второй электрон. На преодоление этого отталкивания дол-ж а быть затрачена энергия. [29]
Таким образом, в сумме при отнятии всех трех электронов будет затрачено 7 478 ат. Если был бы произведен неверный расчет суммирования энергетических характеристик термов нейтрального атома без учета их самопроизвольного смещения, при ионизации получился бы результат, не совпадающий с опытом 0, 198 2 375 2 375 4 948 ат. Присоединение первого электрона к ядру Li3 сопровождается выделением энергии, равной 4 50 ат. [30]
Страницы: 1 2 3