Присутствие - посторонний ион
Cтраница 2
На процесс адсорбции влияет присутствие посторонних ионов. [16]
Величина рН зависит от присутствия других посторонних ионов, поскольку от них зависит ионная сила и, следовательно, коэффициент активности. [17]
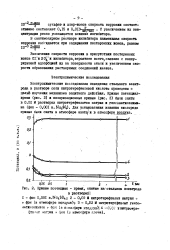 |
Кривые потенциал - время, снятые на. стальном электроде. [18] |
Увеличение скорости коррозии в присутствии посторонних ионов С1ГиЗО и ингибитора, вероятнее всего, связано с конкурирующей адсорбцией их на поверхности стали и увеличением скорости образования растворимых соединений железа. [19]
Чувствительность реакции часто понижается вследствие присутствия посторонних ионов в растворе. Так, прекрасная реакция открытия иона Ti4, основанная на образовании перекисного соединения оранжевого цвета, становится менее чувствительна в присутствии избытка ионов Fe3, обусловливающего желтую окраску раствора. Но если последние замаскировать прибавлением умеренного количества фосфорной кислоты, образующей с ними бесцветные комплексные ионы [ Fe ( PO4) 2 ] 3, то чувствительность реакции на Ti4 с Н2Оо сильно повышается. [20]
Такие электролиты мало чувствительны к присутствию посторонних ионов. Обычно для увеличения электрической проводимости электролита к раствору добавляют соли калия в виде сульфатов, фосфатов, нитратов, цитратов, тартратов, лактатов, бензосульфонатов. Кроме соединений серебра в электролите часто присутствуют и ионы других металлов ( никеля, кобальта), правда, покрытия от этого становятся более хрупкими, хотя и более блестящими. Добавление солей титана делает покрытие более блестящим. Зеркально-блестящими становятся покрытия, когда кроме солей титана еще присутствует селен - тогда покрытия приобретают цвет золота. [21]
В реальных условиях, в присутствии посторонних ионов ( воз-хжно многозарядных), а также в кислой или в щелочной среде иная сила раствора может быть весьма значительной и может [ азывать заметное влияние на величину активности. Поэтому танциалы, найденные в реальных условиях, в некоторых учаях сильно отличаются от нормальных. [22]
 |
Зависимость удельной вязкости водного раствора полиамфолита от рН раствора. [23] |
Изоточки растворов полиамфолитов очень чувствительны к присутствию посторонних ионов, способных сорбироваться на цепях полиамфолита. [24]
В тех случаях, когда в присутствии постороннего иона чувствительность данной реакции снижается, Малисса рекомендует различать абсолютную чувствител ьность Da, относящуюся к случаю, когда в растворе находится лишь один открываемый ион, и практическую чувств и тельностьОр для случая, когда раствор содержит мешающие вещества. [25]
На эффективность действия ингибиторов большое влияние оказывает присутствие посторонних ионов в растворе. Чем выше концентрация агрессивных ионов в растворе, тем выше должна быть и концентрация ингибитора. [26]
Так как на величину растворимости оказывает существенное влияние присутствие посторонних ионов, то все определения необходимо выполнять при постоянной ионной силе ( стр. [27]
Скорость коррозии зависит от концентрации, температуры, присутствия посторонних ионов и воздуха. [28]
Отсутствие нижней границы смешиваемости и независимость коэффициента кристаллизации от присутствия посторонних ионов, казалось, делали вероятным образование в этом случае истинных смешанных кристаллов, но тогда коэффициент кристаллизации должен был бы оставаться постоянным в широком интервале концентрации распределяющегося вещества. [29]
Морфология, состав и дисперсность кристаллов гидросиликатов кальция изменяются в присутствии посторонних ионов в водном растворе и в кристаллах алита. Так, гидратация C3S замедляется в присутствии Са ( ОН) 2, С3А и значительно ускоряется в присутствии CaC z и других хлоридов, бромидов, нитритов, сульфатов, карбонатов, щелочных металлов и гипса. Ускорение реакции обусловливается уменьшением длительности индукционного периода гидратации за счет интенсификации процесса образования зародышей кристаллов новых гидратных фаз. [30]
Страницы: 1 2 3 4