Присутствие - буфер
Cтраница 2
 |
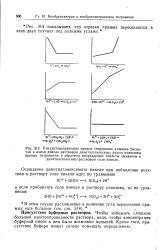
Изменение рН при титровании гидразина соляной кислотой. [16] |
Приведенные данные яснэ показывают, что ни один индикатор не дает возможности точно отметить конечную точку при титровании гидразина стандартной кислотой, если даже проводить титрование в присутствии буферов. Особенно это относится к тем случаям, когда концентрация гидразина ( и стандартной кислоты) сравнительно мала или сильно различается для образцов данной серии, как это может иметь место при проведении массовых анализов. [17]
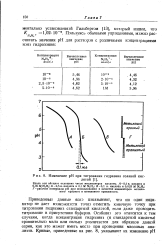
Наибольший урон наносится озерам, в которых вода обладает слабыми буферными свойствами. В присутствии природных щелочных буферов кислые соединения, приносимые дождем ( большей частью серная и азотная кислоты, в меньших количествах органические кислоты), нейтрализуются. Однако озера, лежащие на гранитных ( кислых) породах, весьма подвержены действию попадающих в них кислот, способных переводить в раствор ионы таких металлов, как алюминий и марганец, что может повлечь подавление роста растений и водорослей, а в некоторых озерах - сокращение или вообще исчезновение популяций рыб. Значительный ущерб наносят кислотные дожди и растительности, причем проявление их влияния может быть самым различным - от дефолиации до разрушения тонкой корневой системы. [18]
Чтобы избежать слишком большой электропроводности раствора, надо, чтобы концентрация буферной смеси в нем была возможно меньшей. Кроме того присутствие буфера может сильно помешать определению. [20]
Чтобы избежать слишком большой электропроводности раствора, надо, чтобы концентрация буферной смеси в нем была возможно меньшей. Кроме того, присутствие буфера может сильно помешать определению. [22]
Напомним, что этой буферной смесью постоянно пользуются в качественном анализе, например при отделении катионов II группы от катионов I трупы, а также катионов III группы от катионов II и I групп. В обоих случаях присутствие аммиачного буфера предупреждает выпадение в осадок гидроокиси ( или основного карбоната) магния, произведение растворимости которой при рН - 9 не достигается. [23]
Напомним, что этой буферной смесью постоянно пользуются в качественном анализе, например при отделении катионов II группы от катионов I трупы, а также катионов III группы от катионов II и I групп. В обоих случаях присутствие аммиачного буфера предупреждает выпадение в осадок гидроокиси ( или основного карбоната) 1 магния, произведение растворимости которой при pHss9 не достигается. [24]
Напомним, что этой буферной смесью постоянно пользуются в качественном анализе, например при отделении катионов II группы от катионов I группы, а также катионов III группы от катионов II и I групп. В обоих случаях присутствие аммиачного буфера предупреждает выпадение в осадок гидроокиси ( или ос -: новного карбоната) магния, произведение растворимости которой при рН - 9 не достигается. [25]
Было опубликовано несколько работ по изучению солевых эффектов, позволяющих провести соответствующие вычисления. Однако реакции обычно проводили в присутствии буфера, добавленного для контроля рН, что создавало определенные трудности в интерпретации. Если буфер определяет концентрацию реагирующих противоионов, не удается определить величину /, и по меньшей мере одна из компонент буфера может взаимодействовать с мицеллами, изменяя их свойства неконтролируемым и неизвестным образом. [26]
Как показали исследования, скорости растворения и скорости гидролиза легкогидролизуемых полисахаридов растительных тканей не идентичны. Так, если нагревать растительную ткань в воде в присутствии буфера, обеспечивающего сохранение нейтральной среды, часть гемицеллюлоз переходит в раствор в почти неизмененном виде. В присутствии кислого катализатора растворимая часть гемицеллюлоз также переходит в раствор и начинает гидролизоваться в растворе. Одновременно в раствор переходят обломки молекул гемицеллюлоз, а также отдельные моносахариды, образовавшиеся в результате гидролиза твердого остатка. [28]
В водной среде формы H2In -, HIn2 - и 1п3 - имеют красную, синюю и оранжевую окраску соответственно. Большинство титрований с ЭДТА с применением эриохрома черного Т проводят в присутствии буфера, например смесь аммиака с хлоридом аммония, рН которого 8 - 10; доминирующей формой свободного индикатора является обычно анион HIn2 - с ярко-синей окраской. Кроме того, эриохром черный Т соединяется со многими катионами металлов, приведенными в табл. 6 - 1, с образованием устойчивых комплексов состава 1: 1, окрашенных в винно-красный цвет. [29]
Эти реакции обычно проводятся в растворителях ( например, метиленхлориде) и в отсутствие буфера протекают экзотермич-но с большей скоростью, чем с надмуравьиной кислотой; при этом из высших олефииов даже при значительно более низкой температуре эфиры гликолей получаются с хорошим выходом. В том случае, когда эпоксидное соединение является целевым продуктом, реакция проводится в присутствии буфера ( например, карбоната или бикарбоната натрия для обычных олефинов и динатрий фосфата - для олефннов с электроотрицательными заместителями) и выход продукта обычно высокий. [30]
Страницы: 1 2 3 4