Присутствие - нейтральная соль
Cтраница 1
Присутствие нейтральных солей в растворах, содержащих органические вещества, сказывается на адсорбируемости неэлектролитов не неоднозначно, так как может повышать, понижать адсорбируемость либо не влиять на нее. [1]
В присутствии нейтральных солей величина рН, характеризующая изоэлектрическую точку амфолига, обычно, или уменьшается, или увеличивается. Этот сдвиг объясняется неодинаковой адсорбцией аниона и катиона прибавленной соли. [2]
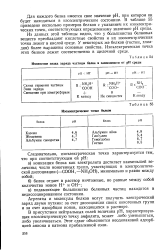 |
Изменение знака заряда частицы белка в зависимости от рН среды. [3] |
В присутствии нейтральных солей величина рН, характеризующая изоэлектрическую точку амфолита, может либо уменьшаться, либо увеличиваться. Этот сдвиг объясняется неодинаковой адсорбцией аниона и катиона прибавленной соли. [4]
В присутствии нейтральных солей в растворе реакционная способность веществ изменяется. Следует ожидать, что ионная атмосфера будет оказывать влияние на процесс столкновения ионов; в свою очередь при наличии соли ионная атмосфера будет изменяться. Число столкновений между ионами противоположного по знаку заряда увеличивается в присутствии солей, которые способствуют электростатическому притяжению, и уменьшается при действии солей, видоизменяющих ионную атмосферу так, что электростатическое притяжение уменьшается. [5]
В присутствии нейтральных солей в растворе реакционная способность веществ изменяется. Следует ожидать -, что ионная атмосфера будет оказывать влияние на процесс столкновения ионов; в свою очередь при наличии соли донная атмосфера будет изменяться. Число столкновений между ионами противоположного по знаку заряда увеличивается в присутствии солей, которые способствуют электростатическому притяжению, и уменьшается при действии солей, видоизменяющих ионную атмосферу так, что электростатическое притяжение уменьшается. [6]
В присутствии нейтральных солей в растворе реакционная способность веществ изменяется. Следует ожидать, что ионная атмосфера будет оказывать влияние на процесс столкновения ионов; в свою очередь при наличии соли ионная атмосфера будет изменяться. Число столкновений между ионами противоположного по знаку заряда увеличивается в присутствии солей, которые способствуют электростатическому притяжению, и уменьшается при действии солей, видоизменяющих ионную атмосферу так, что электростатическое притяжение уменьшается. [7]
В присутствии нейтральных солей в растворе реакционная способность веществ изменяется. Следует ожидать, что ионная атмосфера будет оказывать влияние на процесс столкновения ионов; в свою очередь при наличии соли ионная атмосфера будет изменяться. Число столкновений между ионами противоположного по знаку заряда увеличивается в присутствии солей, которые, способствуют электростатическому притяжению, и уменьшается при действии солей, видоизменяющих ионную атмосферу так, что электростатическое притяжение уменьшается. [8]
В присутствии нейтральных солей в растворе реакционная способность веществ изменяется. Следует ожидать, что ионная атмосфера будет оказывать влияние на процесс столкновения ионов; в свою очередь при наличии соли ионная атмосфера будет изменяться. Число столкновений между ионами противоположного по знаку заряда увеличивается в присутствии солей, которые способствуют электростатическому притяжению, и уменьшается при действии солей, видоизменяющих ионную атмосферу так, что электростатическое притяжение уменьшается. [9]
Особенно сказывается присутствие нейтральных солей, которые в прежних исследованиях окислительно-восстановительных потенциалов часто добавлялись к раствору; они увеличивают ионную силу и, следовательно, имеют заметное влияние на потенциал, даже если отношение количеств окисленных и восстановленных форм вещества остается при этом постоянным. [10]
Соленость обусловливается присутствием нейтральных солей таких, как хлориды и сульфаты кальция, магния, натрия и калия. [11]
Простое титрование катионита в присутствии нейтральной соли дает возможность установить обменную емкость, соответствующую определенному интервалу значений рН раствора в зависимости от применяемого индикатора, и показывает содержание активных групп в катионите. [12]
Слабокислые растворы белков в присутствии нейтральных солей ( например, NaC) при кипячении свертываются. Проба с кипячением в присутствие разбавленной уксусной кислоты и NaCl дает возможность открыть белок при наль ии одной его части на 100 000 частей воды. [13]
Слабокислые растворы белков в присутствии нейтральных солей ( например, NaCl) при кипячении свертываются. Обычно для под-кисления пользуются разбавленной уксусной кислотой. Крепкие минеральные кислоты, за исключением HN03, при этой реакции могут вызывать образование альбумина-тов, растворимых в воде, и поэтому обычно эти кислоты применять не следует. Проба с кипячением в присутствии разбавленной уксусной кислоты и NaCl дает возможность открыть белок при наличии одной его части на 100 000 частей воды. [14]
Слабокислые растворы белков в присутствии нейтральных солей при кипячении свертываются. Обычно для подкисления пользуются разбавленной уксусной кислотой. [15]
Страницы: 1 2 3 4