Присутствие - фермент
Cтраница 1
Присутствие ферментов в ничтожно малых количествах способно расщеплять огромные количества реагирующих веществ. Так, 1 г кристаллического пепсина расщепляет 50 кг коагулированного яичного белка, а 1 г кристаллического ренина свертывает 72 т молока. Фермент пероксидаза, который ускоряет окисление субстрата за счет перекиси водорода, проявляет свою активность при разбавлении 1 вес. [1]
 |
Ферменты часто катализируют последовательно протекающие химические реакции. [2] |
В присутствии ферментов за какие-то секунды протекают сложные последовательности реакций, для проведения которых в химической лаборатории потребовались бы дни, недели или месяцы работы. Кроме того, реакции, катализируемые ферментами, идут со 100 % - ным выходом и без образования побочных продуктов. В то же время известно, что реакции, которые проводят в лаборатории химики-органики, почти всегда сопровождаются образованием одного или нескольких побочных продуктов. [3]
В присутствии фермента кофер-мент NADH избирательно отрывает атом водорода НА только с задней стороны плоскости карбонильной группы, причем образуется хиральный спирт, в котором метиленовые атомы становятся диастереотопными. Однако метальные атомы неразличимы для фермента и называются гомотопными. [4]
В присутствии фермента, выделенного из печени свиньи и названного Кантони никотинамидметилферазой ( фермент, вызывающий трансметилирование), этот активный метионин метилировал никотинамид до N-метилникотинамида в отсутствие аденозинтрифосфата или любого иного фосфата, содержащего богатые энергией связи ( см. стр. [5]
В присутствии ферментов жир одновременно подвергается гидролитическому расщеплению и окислению освобожденных кислот. В процессе микробиологического распада белков выделяется аммиак; со свободными жирными кислотами он образует аммонийные соли. [6]
В присутствии фермента редуктазы молоко, окрашенное метиленовой синью, обесцвечивается, так как редуктаза восстанавливает метиленовую синь, переводя ее в бесцветную лейкоформу. Свежевыдоенное молоко восстанавливает метиленовую синь медленно. С увеличением числа бактерий в молоке скорость восстановления метиленовой сини возрастает. На скорости восстановления в молоке метиленовой сини и основано примерное определение в нем численности бактерии и степени свежести молока - его качества. Однако строгой зависимости между числом бактерий и временем обесцвечивания в нем метиленовой сини нет, так как разные виды бактерий выделяют неодинаковое количество редуктазы. [7]
В присутствии фермента ТГФ-форми-лазы и АТФ формиат реагирует с ТГФ, образуя № - формил - ТГФ ( фиг. [8]
Аминокислота в присутствии тканевого фермента окисляется путем дегидрирования в соответствующую иминокислоту. [9]
 |
Влияние температуры на ак - [ IMAGE ] Влияние рН на активность тивность гидрогеназы лактатдегидрогеназы. [10] |
Некоторые вещества в присутствии ферментов конкурируют с субстратом. Обычно это наблюдается при попадании в сферу действия фермента структурных аналогов субстрата. Такие вещества называют субстратными антиметаболитами. Так, сукци-натдегидрогеназа катализирует превращение янтарной кислоты в фумарат. [11]
Водой гидролизуется в присутствии фермента мальтазы до D-глкжозы. Систематическое название указывает на наличие гликозидной связи между имеющим а-конфигурацию атомом С1 одного остатка глюкозы и атомом С4 другого остатка. [12]
Водой гидролизуется в присутствии фермента мальтозы до D-глкжозы. Систематическое название указывает на наличие гликозиднои связи между имеющим а-конфигурацию атомом С1 одного остатка глюкозы и атомом С4 другого остатка. [13]
ХС Гидролиз в присутствии фермента лактазы ( р-глюкозидазы) приводит к образованию Отгалактозы и о-глюкозы. [14]
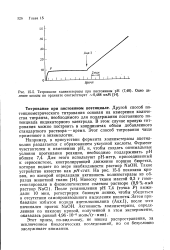 |
Титрование холинэстеразы при постоянном рН ( 7 40. Одно деление шкалы по ординате соответствует - 0 488 мкМ.. [15] |
Страницы: 1 2 3 4