Присутствие - гидроперекись
Cтраница 1
Присутствие гидроперекиси было доказано качественно. [1]
В присутствии гидроперекиси трет. [2]
В присутствии гидроперекисей инициирование реакций происходит за счет свободных радикалов, образующихся вследствие распада гидроперекисей; скорость распада гидроперекиси значительно ниже скорости полимеризации. [3]
В присутствии гидроперекиси ацетила хлористый винил конденсируется с сернистым ангидридом. Рентгеновское исследование показало вполне определенную упорядоченность в структуре, и было сообщено [25], что это соединение содержит 2 молекулы олефина на молекулу сернистого ангидрида. При нагревании теряются и сернистый ангидрид и хлористый водород. Упоминается также об устойчивости этого соединения к действию концентрированной азотной кислоты. [4]
В присутствии гидроперекиси углеводородов и щелочного реагента, например бикарбоната натрия, повышается выход кетонов и спиртов. [5]
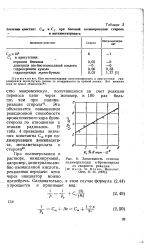 |
Зависимость степени полимеризации я-бромстирола. [6] |
При полимеризации метилметакрилата в присутствии гидроперекиси mpem - бутила данные не укладываются на прямой линии. [7]
Немного лучшие результаты получаются в присутствии гидроперекисей диизопрошглбензола, циклогекаилбевзола ш 2-хлор - 1 4-диизопропилбензола. [8]
При окислении цетана с 3-метилбензтиофеном обнаружено присутствие гидроперекисей в количествах от 0 11 до 0 23 мг O2 / I мл. [9]
В определение карбонильных соединений вносит ошибку присутствие гидроперекисей и ацилперекисей. Если в анализируемой смеси присутствуют перекиси, то рекомендуется удалять их перед оксимированием, обрабатывая навеску раствором щелочи. [10]
Для инициирования сополимеризации дивинила и стирола в присутствии гидроперекисей была предложена система, в которой комплексообразователем является соль окисного железа этилендиаминтетрауксусной кислоты в комбинации с гидразином или сульфидом натрия в качестве восстановителей. Окисное железо в этом комплексе медленно восстанавливается гидразином или сернистым натрием в закисное, которое немедленно реагирует с гидроперекисью с образованием свободных радикалов и ионов окисного железа, причем последние вновь связываются с этилендиаминтетрауксусной кислотой в комплекс. [11]
Скорость окисления тетрагидрофурана практически не изменяется в присутствии гидроперекисей различных эфиров и углеводородов, дающих вторичные пероксирадикалы ( табл. 36), а константы скорости реакций продолжения и обрыва цепей для вторичных пероксирадикалов эфиров и углеводородов одинаковы. Результаты, полученные с трег-бутилгидропере-кисью, подтверждают, что третичные пероксирадикалы менее реакционноспособны, чем вторичные, в реакции продолжения цепи. [12]
Наблюдаемые изменения в спектре ЭПР хелата ( 1) в присутствии гидроперекиси позволяют сделать вывод о дополнительной координации гидроперекиси по пятому и шестому или только по пятому координационному месту металла. [13]
Хелаты 1 3-дикетонов Си, Сг, Со и Fe в присутствии гидроперекиси трет-бутила исследованы как инициаторы полимеризации стирола при умеренных температурах ( 50 С) [ N. [14]
Было установлено, что при взаимодействии аппрета и указанной смеси в присутствии гидроперекиси кумола даже при 80 С винильные группы аппрета не-вступают в реакцию. Это может служить доказательством отсутствия химического взаимодействия аппрета с полиэфирной смолой при отверждении. Однако тщательный подбор мономеров, смолы, аппрета, температурного режима отверждения и других параметров процесса в принципе может привести к образованию химических связей и улучшению свойств стеклопластика. [15]
Страницы: 1 2 3 4