Взаимное притяжение - молекула
Cтраница 1
Взаимное притяжение молекул приводит к образованию между ними более или менее слабых связей, и это явление часто называют ассоциацией. Однако такой термин в данном случае не однозначен, поскольку вообще могут существовать разные типы межмолекулярных связей. Теоретические исследования [12] показывают, что в жидкостях существуют два основных типа молекулярных ассоциаций. В одних случаях под действием межмолекулярных сил образуются агрегаты ( комплексы), состоящие из нескольких молекул, которые движутся как единое кинетическое целое. В других случаях под ассоциацией понимают только наличие корреляции между положением молекул и межмолекулярными силами, которая незначительно влияет на движение отдельных молекул. [1]
Взаимное притяжение молекул усиливается с уменьшением расстояния между ними. При этом возрастает также и доля пространства, занимаемого самими молекулами. [2]
Взаимное притяжение молекул эквивалентно внутреннему ( когезионному) давлению, так как оно, подобно внешнему давлению р, стремится уменьшить объем газа. [3]
Взаимное притяжение молекул одной жидкости молекулами другой жидкости обусловливает явление адгезии между ними. [4]
Взаимное притяжение молекул усиливается с уменьшением расстояния между ними. При этом возрастает также и доля пространства, занимаемого самими молекулами. [5]
Взаимное притяжение молекул препятствует разле-танию их и, следовательно, действует в том же направлении, что и внешнее давление, удерживающее газ в заданном объеме. При определении действующих сил взаимного притяжения молекул достаточно в первом приближении к внешнему давлению р прибавить некоторый добавочный член р, который называется внутренним или молекулярным давлением. [6]
Взаимное притяжение молекул усиливается с уменьшением расстояния между ними. При этом возрастает также и доля пространства, занимаемого самими молекулами. [7]
Взаимное притяжение молекул ВЧЯИМНПР притяжение между молекулами ( явление когезии) носит сложный характер. [8]
Взаимное притяжение молекул газа обусловлено действием сил Ван-дер - Ваальса. Силы эти, вызывая уменьшение объема газа, действуют на него как некоторое добавочное давление к внешнему, которое называют внутренним давлением. [9]
Взаимным притяжением молекул обусловливается наличие запаса потенциальной энергии в газе. [10]
Силы взаимного притяжения молекул в жидкостях значительно слабее, чем в твердых телах. [11]
Причину взаимного притяжения молекул, не связанного с наличием электрических диполей, впервые нашел Лондон - тот самый физик, который вместе с Гайтлером создал теорию химической связи ( стр. Лондон показал, что любые атомы или молекулы должны притягиваться друг к другу, так как электроны в них не неподвижны. Движение электронов приводит к появлению не постоянных, но переменных диполей, которые и притягиваются друг к другу. Периодическое движение электронов в соседних молекулах создает их резонанс и вызывает появление сил притяжения. [12]
Энергия взаимного притяжения молекул для всех указанных типов взаимодействия приблизительно обратно пропорциональна шестой степени расстояния между молекулами. Между молекулами ассоциированной жидкости образуются кратковременные непостоянные связи. К таким связям относится водородная связь, которая создается за счет электростатического притяжения протона одной молекулы к аниону или электроотрицательному атому ( главным образом к атомам фтора, кислорода, азота, хлора) другой молекулы. [13]
Энергия взаимного притяжения молекул для всех указанных типов взаимодействия приблизительно обратно пропорциональна шестой степени расстояния между молекула-ми. Между молекулами ассоциированной жидкости образуются кратковременные непостоянные связи. К таким связям относится водородная связь, которая создается за счет электростатического притяжения протона одной молекулы к аниону или электроотрицательному атому ( главным образом к атомам фтора, кислорода, азота, хлора) другой молекулы. [14]
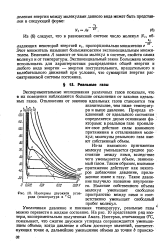 |
Изотермы двуокиси углерода ( температура в С. [15] |
Страницы: 1 2 3 4