Про-тонирование
Cтраница 3
Реакция протекает в присутствии фосфорной кислоты или кислот Льюиса Активация ацетилена на первой стадии реакции достигается, по-видимому, не путем образования п-комплексов с ионами металлов, а про-тонированием. [31]
Реакция конкурирует с Sjrl-реакцией ( см. ОХ 6), поскольку обе имеют одну и ту же определяющую скорость стадию ( 1) ( при X ОН предварительно происходит про-тонирование): образование карбониевого катиона. На завершающей стадии ( 2) основание отщепляет от катиона протон, тогда как в случае 5wl - реакции нуклеофил со своей парой электронов образует о-связь с электронодефицитньзд атомом углерода. [32]
Константы устойчивости комплексов вида МлНдХГ либо константы равновесия реакций их образования могут быть рассчитаны с использованием методов, рассмотренных при обсуждении реакций образования смешанных комплексов и реакций, осложненных про-тонированием лигандов. [33]
Сравнивая результаты двух предыдущих параграфов, можно прийти к следующему выводу: протонирование и-ксилола как по атому С1, так и по атому G2 дает катион, который стабилизируется делокализацией по кольцу и одной метильной группой, тогда как протонирование мезитилена по атому С2 ( который, как мы выяснили, является предпочтительным местом про-тонирования) дает катион, который стабилизируется делокализацией по кольцу и тремя метальными группами. Следовательно, мезитилен, протони-рованный по С2, более устойчив, чем n - ксилол, протонированный по С1 или по С2; а раз так, то мезитилен даст большую концентрацию соли в жидком фтористом водороде, чем гс-ксилол. [34]
Основность карбоновой кислоты определяется ее способностью присоединять протон. При про-тонировании протон присоединяется к карбонильному кислороду с образованием протонированной молекулы карбоновой кислоты. [35]
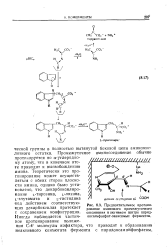 |
Предпочтительное протонирование нминового промежуточного соединения в активном центре пнрид-оксальфосфат-зависнмых ферментов. [36] |
Промежуточное иминосоединение обычно протонируется по а-углеродно-му атому, что в конечном итоге приводит к высвобождению амина. Теоретически это про-тонирование может осуществляться с обеих сторон плоскости имина, однако было установлено, что декарбокоилиро-вание L-тирозина, ь-лизина, L-глутамата и ь-гистидина под действием соответствующих декарбоксилаз протекает с сохранением конфигурации. Иногда наблюдается частичное протонирование положения С-4 молекулы кофактора, что приводит к образованию неактивного конъюгата фермента с пиридоксаминфосфатом. [37]
Была сделана пробная расшифровка сигналов гетеро-циклов соединений путем сравнения сдвигов диссоциированных пуринов со сдвигами соединений соответствующих пуринов с моно-и трифосфатами рибозы. Изменение химических сдвигов при про-тонировании было использовано для получения данных о структуре протонированных соединений. [38]
В этом случае скоростьопределяющей стадией является образование карбкатиона. Роль кислотного катализа сводится к про-тонированию атома кислорода, в результате чего в качестве уходящей группы выступает не карбанион, а нейтральная молекула карбоновой кислоты. Таким образом, этот механизм фактически эквивалентен механизму мономолекулярного нуклеофильного замещения 5 1 и подчиняется тем же закономерностям. [39]
Карбанионы чаще всего получают в средах с низкой диэлектрической проницаемостью, где они существуют в виде ионных пар и агрегатов ионных пар. Многое известно о механизме образования и про-тонирования этих частиц, включая данные о влиянии растворителя. Однако здесь активную роль играет противоион, и полностью эта тема рассмотрена в гл. [40]
 |
Нуклеофильное замещение в производных карбоновых кислот. [41] |
Вследствие поляризации карбонильной группы карбонильные соединения склонны к атаке нуклеофилами ( разд. Добавки кислоты могут катализировать реакцию благодаря про-тонированию карбонильного атома кислорода я обусловленному им усилению поляризации. Однако слишком большое количество кислоты может подавлять реакцию, поскольку протони-руется также нуклеофил, который становится йереакционноспо-собным. [42]
Обратный изотопный эффект растворителя характерен для реакций со специфическим кислотным катализом. Следовательно, протонирование диазоуксусного эфира в противоположность про-тонированию дифенилдиазометана должно быть обратимым. Это вполне вероятно, поскольку при разложении протонированного диазоуксусного эфира положительный заряд локализуется рядом с частично положительно заряженным карбонильным атомом углерода. Эта неблагоприятная ситуация замедляет распад протонированного диазоуксусного эфира по сравнению с протониро-ванным дифенилдиазометаном - реакцией, в которой положительный заряд в образующемся дифенилметильном катионе полностью делокалпзован. Следовательно, эфир этоксиуксусной кислоты содержит более одного D-атома. [43]
Возможность образования изомера с открытой цепью ( 27) обсуждалась и в данном случае [. ], но были получены дальнейшие доказательства [10], в пользу хпно. Структура с открытой цепью ( 27) при про-тонировании должна была бы давать батохромное смещение, как это имеет место 1ля производных хинолина ( см. разд. [44]
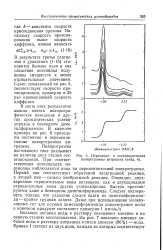 |
Переменно - и постоянноточная полярограммы антрацена ( 4. [45] |
Страницы: 1 2 3 4