Анализируемая проба - вода
Cтраница 3
Для определения жесткости воды по кальцию в 100 мл анализируемой пробы воды вливают концентрированный раствор щелочи рН 12, свежеприготовленный насыщенный раствор мурексида до пурпурно-красной окраски. Титруют раствором коплексона III до появления сине-фиолетовой окраски. [31]
Трилонометрическое определение жесткости воды предотвращает ошибку определения, связанную с необходимостью нейтрализации анализируемой пробы воды. Комплексонометрический метод допускает прямое титрование, в то время как в старых методах определения жесткости воды применялось обратное титрование. Широкое распространение комплексонометрических методов связано с постоянством состава образующихся внутрикомплексных соединений, что не наблюдается при других реакциях комплексо-образования. [32]
Комплексонометрический метод определения жесткости воды исключает ошибку, связанную с необходимостью нейтрализации анализируемой пробы воды. Он допускает прямое титрование воды, в то время как в прежних методах применялось обратное титрование. Широкое распространение комплексонометрических методов связано с постоянством состава образующихся внутрикомплексных соединений. [33]
Отметим, что воспроизводимость, полученная на стандартных растворах, может отличаться от полученной на анализируемой пробе воды. Если расхождение значимо, нужно убедиться в отсутствии возможного загрязнения или потерь из анализируемой пробы. [34]
Все вновь разработанные приборы действуют на основе современных физико-химических методов, позволяющих в многокомпонентных растворах, каковыми являются анализируемые пробы воды, пара и конденсата электростанций, определять микроконцентрации одного или группы компонентов. [35]
К - поправка к нормальности раствора трилона Б; V - объем раствора трилона Б, израсходованный на титрование анализируемой пробы воды, мл; V - объем пробы воды, взятой на анализ, мл. [36]
Данные таблицы I показывают, что рассматриваемый визуальный метод в широком диапазоне колебаний относительного содержания нефти ( нефтепродуктов) в анализируемой пробе воды позволяет получать результаты весьма близкие к тем данный, которые дает метод колориметрии. Причем сходимость результатов параллельных анализов по двум сравниваемым методам также примерно одинакова. [37]
В колбу с пробкой из самозатягивающейся резины, взвешенную с точностью до 0 0002 г и охлажденную в смеси льда с водой до 5 С, помещают около 100 мл анализируемой пробы эфирной воды и взвешивают с той же точностью. Затем в пробу вводят шприцем, прокалывая иглой пробку, 0 03 - 0 05 мл диэтилового эфира и снова взвешивают. После осторожного и тщательного перемешивания содержимого колбы отбирают полученную смесь микрошприцем и вводят в хроматограф. Снимают не менее трех хроматограмм и определяют площади пиков ( см. стр. [38]
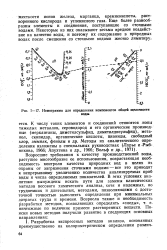 |
Номограмма для определения компонентов общей щелочности. [39] |
Возросшие требования к качеству производственной воды, растущее многообразие ее использования, возрастающая необходимость контроля качества природных вод в целях их охраны от загрязнения сточными водами - все это приводит к непрерывному увеличению количества анализируемых проб воды и числа определяемых показателей. В этих условиях аналитики вынуждены искать пути для замены классических методов весового химического анализа, хотя и надежных, но трудоемких и длительных, методами, позволяющими с достаточной точностью выполнять определения при минимальных затратах труда и времени. [40]
В мерные колбы вводят 0; 0 50; 1 00; 2 00; 5 00; 10 00; 15 00 мл рабочего стандартного раствора ванадия Объем стандартов доводят дистиллированной водой до объема анализируемой пробы воды. Содержание V51 в стандартах составляет 0; 0 0005; 0 001: 0 002; 0 005; 0 010; 0 015 мг / 10 мл раствора. [41]
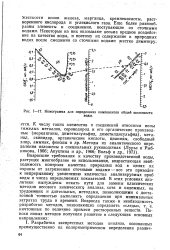 |
Номограмма для определения компонентов общей щелочности. [42] |
Возросшие требования к качеству производственной воды, растущее многообразие ее использования, возрастающая неЬб - ходимость контроля качества природных вод в целях их охраны от загрязнения сточными водами - все это приводит к непрерывному увеличению количества анализируемых проб воды и числа определяемых показателей. В этих условиях аналитики вынуждены искать пути для замены классических методов весового химического анализа, хотя н надежных, HQ трудоемких и длительных, методами, позволяющими с достаточной точностью выполнять определения при минимальных затратах труда и времени. [43]
Ai - поправка для приведения концентрации раствора комплексона к точно 0 025 М; b - объем 0 025 М раствора соли магния, израсходованного на титрование избытка комплексона, мл; Kz - поправка для приведения концентрации раствора соли магния к точно 0 025 М; V - объем анализируемой пробы воды, мл; У. [44]
Ai - поправка для приведения концентрации раствора комплексона к точно 0 025 М; Ь - объем 0 025 М раствора соли магния, израсходованного на титрование избытка комплексона, мл; К - - поправка для приведения концентрации раствора соли магния к точно 0 025 М; V - объем анализируемой пробы воды, мл; V - емкость мерной колбы, куда был переведен раствор после окисления серы до сульфат-ионов, мл; V2 - объем аликвотной порции, взятой для титрования сульфат-ионов, мл; 0 802 - количество серы, эквивалентное I мл 0 025 М раствора, мг; 2 402 - количество SO -, эквивалентное 1 мл 0 025 М раствора, мг. [45]
Страницы: 1 2 3 4