Аликвотная проба
Cтраница 2
Микрошприцем отбирают аликвотные пробы, разбавляют их в 250 раз и измеряют поглощение полученного раствора на спектрофотометре ггри 223 ммк. Удовлетворительные результаты дают полисахариды, хорошо растворимые в воде или легко диспергируемые в горячей воде. [16]
Газохроматографический контроль аликвотных проб раствора показывает, что реакция завершается за 1 - 3 час. [17]
Отбирают пипеткой две аликвотные пробы по 25 мл и наливают в две конические колбы емкостью 250 мл. В колбы добавляют по 75 мл воды и по 2 - 3 капли бромкрезолового зеленого. Пробы титруют раствором едкого натра до перехода окраски индикатора. Затем одну колбу оставляют в качестве свидетеля ( холостая проба), а в другую добавляют 10 - 12 мл ацетона. Выделившуюся от реакции сернокислого гидроксиламина с ацетоном кислоту титруют раствором едкого натра до достижения окраски холостой пробы. [18]
Отбирают пипеткой две аликвотные пробы по 25 мл в конические колбы емкостью 250 мл. В каждую из колб добавляют по 75 мл воды и 2 - 3 капли бромкрезолового зеленого. Пробы титруют раствором едкого натра до перехода окраски индикатора в желтый цвет. Одну колбу оставляют в качестве свидетеля ( холостая проба), а в другую - добгвляют 10 - 12 мл ацетона и титруют выделившуюся кислоту раствором едкого натра до достижения окраски холостой пробы. [19]
К 20 мл аликвотной пробе анализируемого раствора добавляют 0 5 мл не содержащего кислот этиленгликоля и через 10 мин избыток йодистого калия. [20]
В центрифужные пробирки вносят аликвотные пробы диализата ( 1 мл), содержащие 1 5 - 8 0 -у формальдегида, и добавляют 10 мл реактива. Выпавший при этом сульфат свинца отделяют центрифугированием и образующиеся прозрачные растворы переносят в пробирки 1 ( 19 X X 150 мм), нагревают 30 мин на кипящей водяной бане, защищая от света, охлаждают и измеряют поглощение при 570 ммк на спектрофотометре против раствора, полученного в холостом опыте. [21]
При амперометрическом определении цианидов аликвотную пробу раствора плава ( 5 мл), содержащую Ы0 - 2 - ЫО-2М KCN, отбирают в стаканчик для титрования емкостью 20 - 25 мл, добавляют 1 мл 0 1 N раствора КОН, перемешивают в течение 30 - 40 сек и титруют 0 017V раствором AgNO3 с платиновым вращающимся электродом в качестве индикаторного и меркуриодидным электродом сравнения без наложенного напряжения. Показание гальванометра записывают через каждые 15 сек. [22]
Через определенные промежутки времени отбирают аликвотные пробы растворов и измеряют расход периодата и количество выделившейся муравьиной кислоты. Если окисляемый полисахарид дает с водой суспензию, то перед отбором пробы для анализа ее следует энергично взболтать. [23]
Содержание только гипобромит-иона определяют титрованием другой аликвотной пробы 0 1 TV раствором Na3AsO3 до исчезновения желтой окраски иона ВгО -, затем добавляют 25 мл боратного буферного раствора с рН 8 3 и 0 5 мл 0 05 % - ного раствора бромтимолового синего и дотитровывают до перехода окраски из желто-зеленой в сине-зеленую. В оттитрованной пробе определяют бромит. Для этого к ней очень быстро добавляют 5 мл 20 % - ного раствора KJ и выделившийся иод титруют 0 1 N раствором Na3AsO3 по крахмалу. [24]
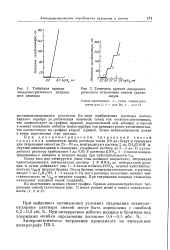 |
Типичная кривая амперометрического титрования цианида.| Типичная кривая амперометрического титрования смесей галогенидов. [25] |
При амперометрическом титровании смесей галогенов аликвотную пробу раствора плава ( 10 мл) берут в стаканчик для титрования емкостью 25 - 30 мл, нейтрализуют раствор 2 мл СН3СООН и, опустив кипятильники в стаканчик, упаривают раствор до 2 - 3 мл. [26]
Свободный галоген определяют в одной аликвотной пробе иодометрическим методом, а в другой его восстанавливают до бромида действием FeS04; смесь галогенидов анализируют поляризационным титрованием. [27]
Железо и медь определяют в отдельных аликвотных пробах фильтрата, полученного в результате мокрого озолеиия. Железо выделяют в виде гидроокиси и определяют колориметрическим методом. Аналогичным образом определяют медь. [28]
В некоторых случаях методика включает отбор аликвотных проб, с последующим их разведением растворителями, используемыми в спектроскопии, что связано с определенными неудобствами. Тем не менее таким простым и точным методом [20] достигается контроль за реакцией, а в ряде случаев этим методом сравнительно быстро и точно удается получить представление о природе продуктов распада или промежуточных соединений. [29]
В некоторых случаях методика включает отбор аликвотных проб с последующим их разведением растворителями, используемыми в спектроскопии, что связано с определенными неудобствами. Тем не менее таким простым и точным методом [20] достигается контроль за реакцией, а в ряде случаев этим методом сравнительно быстро и точно удается получить представление о природе продуктов распада или промежуточных соединений. [30]
Страницы: 1 2 3 4