Ванадат-ион
Cтраница 2
 |
Ориентация ванадат-иона. [16] |
Аналогичным образом было изучено адсорбционное состояние ванадат-ионов. Это означает, что в адсорбированном состоянии заряд на центральном ионе металла остается положительным, а отрицательный заряд оттянут к атомам кислорода на периферию аниона. Сумма зарядов на атомах кислорода в адсорбированном состоянии возрастает по сравнению с зарядом свободного радикала. Это свидетельствует о том, что взаимодействие анионов подобного типа с металлом происходит посредством кислородных атомов. [17]
 |
Температурные и временные параметры для RVO4.| Температурная зависимость интенсивности люминесценции ( 1 и длительности послесвечения ( 2 ортованадатов. [18] |
Интенсивность свечения твердых растворов определяется концентрацией ванадат-ионов. Оптимальная концентрация ионов V034 составляет 25 мол. [19]
При прямом потенциометрическом титровании бихромат - и ванадат-ионов [29, 30] ( восстановление до Сг3 и V02) получаются неточные результаты. [20]
 |
Полярограммы растворов ванадата аммония, бихромата и перманганата калия, снятые на платиновом вращающемся электроде. [21] |
Отсюда следует практический вывод: если в растворе присутствует ванадат-ион, то, снижая кислотность раствора, можно избежать его восстановления на электроде, несмотря на то что в растворе он будет восстанавливаться, если этот раствор титровать каким-либо восстановителем. [22]
Отсюда следует практический вывод: если в растворе пр / гствует ванадат-ион, то, снижая кислотность раствора, можно избежать его восстановления на электроде, несмотря на то что в растворе он будет восстанавливаться, если этот раствор титровать каким-либо восстановителем. [23]
При этом потенциале реактив - четырехвалентный церий и продукт реакции - ванадат-ион восстанавливаются на платиновом электроде. [24]
В одной части определяют ванадий; для этого ванадил-ионы окисляют до ванадат-ионов действием КМп04, избыток которого разрушают щавелевой кислотой. В другой окисляют Cr ( III) и V02 соответственно до Сг207: - и 03 - персульфатно-серебряным методом. Образовавшиеся при этом ионы МпО - восстанавливают до Мп ( П) кипячением раствора с небольшим количеством NaCl. В третьей аликвотной части определяют иарганец. Содержание хрома определяют по разности результатов, полученных при втором и первом титрованиях. [25]
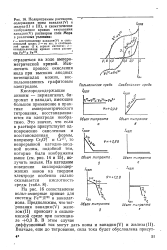 |
Подпрограммы растворов, содержащих ионы ванадия ( V и железа ( II и III, и схематическое изображение кривых титрования ванадия ( V раствором соли Мора в различных условиях. [26] |
На рис. 16 сопоставлены вольт-амперные кривые для системы РеП1 / Рп и ванадат-иона. Предположим, что тит - рования ванадия ( V) железом ( II) проводят в сильнокислой среде при потенциале 0 3 В. [27]
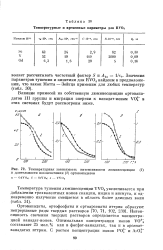 |
Температурные и временные параметры для RVO4.| Температурная зависимость интенсивности люминесценции ( 1 и длительности послесвечения ( 2 ортованадатов. [28] |
Влияние примесей на собственную люминесценцию ортована-датов III группы и миграция энергии к ванадат-ионам VOf в этих системах будут рассмотрены ниже. [29]
Солью ртути ( Hgf) можно титровать пер-манганат-ионы в присутствии бихромат - и ванадат-ионов ( см. Марганец, стр. [30]
Страницы: 1 2 3 4