Продувание - система
Cтраница 3
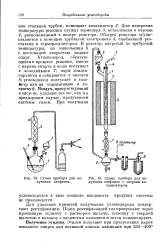 |
Схема прибора для получения олефинов.| Схема прибора для получения олефинов с твердым катализатором. [31] |
Для измерения температуры реакции служит термопара 3, вставленная в карман 4, расположенный в центре реактора. Обогрев реактора осуществляется с помощью трубчатой электропечи 5, снабженной реостатами и терморегулятором. В реактор, нагретый до требуемой температуры, из капельницы 6 с постоянной скоростью подают спирт. Воздух, присутствующий в системе, удаляют так же, как и в предыдущем случае, продуванием системы газом. [32]
На рис. 10.1 и 10.2 показаны приборы двух типов, предназначенные для проведения микрогидрирования. В приборе Огга и Купера70 ( рис. 10.1) объем поглощенного водорода измеряют газовой бюреткой. Методика гидрирования с помощью этого прибора приведена в примере 45 в гл. На рис. 10.3 изображен модифицированный реакционный сосуд для гидрирования. В этом сосуде имеется отверстие для продувания системы водородом и Две отводные трубки, которые можно снабжать пробками с подвешивающимися на них чашечками. Это дает возможность дополнительно вводить образец или катализатор. [33]
Намечается более широко использовать высокотемпературные теплоносители в качестве промежуточных. Такими теплоносителями могут быть синтетические химические композиции и составы на основе минерального масла. К высокотемпературным органическим теплоносителям ( ВОТ) относятся: даутерм ( динил), представляющий эвтектическую смесь дифенила и дифенилокси-да, арохлор ( тетрахлордифенил), глицерин, тетракрези-локоисилан ( тетракрезилсиликат), являющийся представителем кремнийорганических соединений, а также и другие жидкости. Составы на, основе минерального масла не вызывают коррозии металла и не образуют накипи, так как обладают малой минерализацией и высокой щелочностью. Использование термических жидкостей в системе подогрева исключает необходимость продувания системы, предусматриваемого обычно в паровых системах для удаления конденсата. Неполное удаление конденсата в паровых системах подогрева часто является причиной выхода из строя системы при отрицательных температурах окружающей среды. Термические жидкости не изменяют своего физического состояния при температуре от - 12 до 300 С и выше без избыточного давления. Величина избыточного давления будет обусловлена только гидравлическим сопротивлением системы. [34]
Все операции проводят в атмосфере азота. В трубку Шленка помещают 46 3 г ( 0 29 моль) безводного СгС13, 46 3 г ( 1 72 моль) порошка А1, 40 0 г ( 0 30 моль) абсолютно безводного АЮЬ, примерно 5 г сплава Деварда и смесь хорошо растирают стеклянным пестиком. Добавляют еще - 250 мл бензола и тотчас закрывают. Систему однократно продувают СО, доводя давление до 100 бар; для реакции необходимо давление СО порядка 260 бар. По окончании автоклав охлаждают и сжигают избыток СО. После продувания системы азотом автоклав открывают. [35]
При увеличении молярного соотношения каталитическая активность падает. Элементарный анализ продуктов реакции между компонентами катализатора при их молярном соотношении 4: 1, когда каталитическая активность достигает нулевого значения, показал, что средняя валентность титана в системе также равна нулю. Эти результаты находятся в противоречии с данными Фридлендера и Оита [154], согласно которым при комнатной температуре и молярном отношении 4: 1 восстановление четырехвалентного титана происходит лишь в незначительной степени. Однако указанное противоречие кажущееся. Если считать, что методика, использованная в последней работе, а именно продувание системы этиленом перед смешением компонентов катализатора, все-таки приводит к тому, что в действительности компоненты катализатора реагируют в отсутствие этилена, то данные по исчезновению активности при соотношении компонентов катализатора 4: 1, полученные в двух цитированных работах, вполне согласуются. Однако причины отсутствия каталитической активности в обоих случаях различны. При комнатной температуре восстановления вообще не происходит, а при 100 наблюдается полное восстановление. Обе причины представляются достаточными, если принять, что для получения активного катализатора необходимо присутствие металла в промежуточном валентном состоянии. [36]
При увеличении молярного соотношения каталитическая активность падает. Элементарный анализ продуктов реакции между компонентами катализатора при их молярном соотношении 4: 1, когда каталитическая активность достигает нулевого значения, показал, что средняя валентность титана в системе также равна нулю. Эти результаты находятся в противоречии с данными Фридлендера и Опта [154], согласно которым при комнатной температуре и молярном отношении 4: 1 восстановление четырехвалентного титана происходит лишь в незначительной степени. Однако указанное противоречие кажущееся. Если считать, что методика, использованная в последней работе, а именно продувание системы этиленом перед смешением компонентов катализатора, все-таки приводит к тому, что в действительности компоненты катализатора реагируют в отсутствие этилена, то данные по исчезновению активности при соотношении компонентов катализатора 4: 1, полученные в двух цитированных работах, вполне согласуются. Однако причины отсутствия каталитической активности в обоих случаях различны. При комнатной температуре восстановления вообще не происходит, а при 100 наблюдается полное восстановление. Обе причины представляются достаточными, если принять, что для получения активного катализатора необходимо присутствие металла в промежуточном валентном состоянии. [37]
Страницы: 1 2 3