Димерная продукты
Cтраница 3
Имеет значение и структура поверхности графитового анода. Пирографит с другой ориентацией поверхности оказывается менее пригодным для изготовления анода. Оказалось, что при электролизе водных растворов карбоксилатов димерные продукты, характерные для электросинтеза Кольбе, вообще не получаются. [31]
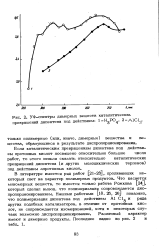 |
УФ-спектры димерных веществ каталитических превращений дипентена под действием. 1 - НдРО, 2. [32] |
В литературе имеется ряд работ [ 21 - 23J, проливающих некоторый свет на характер полимерных продуктов. Что касается мономерных веществ, то имеется только работа Рожкова [ 24, который сделал вывод, что полимеризация сопровождается дис-пропорционированием. Нашими работами 18, 25, 2б ] показано, что полимеризация дипентена под действием Al C1 и ряда других подобных катализаторов, в отличие от протонных кислот, не сопровождается изомеризацией, хотя в некоторых случаях возможно диспропорционирование. Различный характер имеют и димерные продукты. [33]
Ароматические альдегиды и кетоны, как правило, образуют димерные продукты со значительно более высокими выходами, чем алифатические соединения. Некоторые исключения могут быть обусловлены стерическими затруднениями. Однако стерические факторы в большинстве случаев не имеют решающего значения. Так, ацетофенон и бензофенон образуют димерные продукты с почти равными выходами и даже куминоин [120] может быть успешно подвергнут катодной гидро-димеризации, несмотря на явные пространственные затруднения для образования новой связи С-С. [34]
Высшие а-олефипы ведут себя также. В начале превращения они быстро димери-зуготся. Наряду с этим часть мономеров, еще не успевших димеризоваться, претерпевает изомеризацию двойных связей. Из находящихся в равновесии изомеров только изомеры-1 превращаются в димерные продукты, но эти олефины всегда имеются только в ограниченном количестве, а установление равновесия требует времени. Поэтому процесс этот протекает медленно. [35]
Высшие а-олефины ведут себя также. В начале превращения они быстро димери-зуются. Наряду с этим часть мономеров, еще не успевших димеризоваться, претерпевает изомеризацию двойных связей. Из находящихся в равновесии изомеров только изомеры-1 превращаются в димерные продукты, но эти олефины всегда имеются только в ограниченном количестве, а установление равновесия требует времени. Поэтому процесс этот протекает медленно. [36]
Попытки получить полимеры из замещенных 2 - и 3-тетрагидрофура-нов в условиях, когда сам тетрагидрофуран легко полимеризуется, оказались безуспешными. Однако 2-метилтетрагидрофуран вступает в реакции совместной полимеризации с другими циклическими эфирами [ эиихлоргидри-ном н 3 3-бис ( хлорметил) - оксациклобутаном ] [ I s h i g a k i A. Композиционный анализ сополимера показывает, что при высокой концентрации 2-метилтетра-гидрофурана в смеси мономеров он может входить в сополимер в виде блоков, что указывает на принципиальную способность 2-метилтетрагидро-фурана к гомополимеризации. Тем не менее при гомополимеризации этого мономера высокомолекулярных полимеров получить не удается, образуются лишь димерные продукты [ Alexander К. [37]
При стоянии на воздухе и свету пиррол подвергается самоокислению с образованием красно-коричневых, затем черных пигментов ( пиррол черный) [74]; скорость окисления возрастает при наличии алкильных заместителей. Точная природа пигментов неизвестна, но начальные продукты реакции, вероятно, очень похожи на те, что образуются при действии пероксидов и перокси-кислот. Так, при действии концентрированного пероксида водорода пиррол с умеренным выходом дает таутомерную смесь 2-ок-со - А3 - и - А4 - пирролинов ( 76) и ( 77); УУ-метил - и 3-метилпирролы превращаются в соответствующие 2-оксо - А3 - пирролины. Из черных пигментов выделены также димерные [76] ( 79а) и тримерные [77] ( 80) продукты, которые, вероятно, образуются при нуклеофильном присоединении пиррола к 2-оксо - А4 - пирролинам; подобные димерные продукты можно получать и при автоокислении алкилпирролов [ например, ( 796) ] или W-метилпиррола. [38]
Дайн и Денхартог [73] нашли в алифатических системах сильную зависимость величин gi ( D2) от природы растворителя; например, растворы циклогексана - 12 дают величину gi ( D2), равную 2 6 в пен-тане, ко только 0 28 в н-декане. Поэтому значения gi ( D2) или gi ( H2), даже когда сравниваются сходные растворители, нельзя рассматривать как важные, широко применимые константы. Анализ кинетики показывает, что сильно различающиеся реакции, например перенос возбуждения, ионно-молекулярные реакции, действие слабо возбужденных электронов, могут отвечать формальной кинетике, описывающей наблюдаемую зависимость от растворителя. Однако соответствующие трудности не были обнаружены для бензола-йв в различных ароматических растворителях. Это наводит на мысль, что найденная здесь величина g i ( D2) не зависит от природы смеси. Соответствующие измерения для толуола отсутствуют ( так как димерные продукты из толуола, например бензй. [39]
Полностью отличить радикальные реакции от нерадикальных невозможно, поэтому вычислять абсолютные величины такого разрыва рискованно, но, по-видимому, можно вычислять относительную вероятность разрыва. Исходную точку для таких расчетов задают продукты промежуточного молекулярного веса. Из-за малой величины их выхода они должны образоваться вблизи трека ионизирующей частицы, представляя начальную концентрацию радикалов. Три изомерных углеводорода с одним и тем же числом атомов углерода ( например, 3-ме-тилгексан, 2-метилгексан и - гептан) определяют распределение гексильных радикалов. Это распределение не зависит от взятого триплета изомеров, а также от температуры ( в широком интервале), несмотр я на то что выход этих продуктов изменяется в этом интервале более чем на порядок. Распределение различных групп углеродных атомов дает их относительная концентрация вместе с соответствующей концентрацией гексильных радикалов. Распределение позволяет оценить, в каком соотношении эти радикалы исчезают путем диспропорционирования и в какой степени димерные продукты образуются соединением радикалов. Оценка концентрации гексильных радикалов не очень точна, но ошибка не должна быть значительной. [40]
Полностью отличить радикальные реакции от нерадикальных невозможно, поэтому вычислять абсолютные величины такого разрыва рискованно, но, по-видимому, можно вычислять относительную вероятность разрыва. Исходную точку для таких расчетов задают продукты про межуточного молекулярного веса. Из-за малой величины их выхода они должны образоваться вблизи трека ионизирующей частицы, представляя начальную концентрацию радикалов. Три изомерных углеводорода с одним и тем же числом атомов углерода ( например, 3-ме-тилгексан, 2-метилгексан и н-гептан) определяют распределение гексильных радикалов. Это распределение не зависит от взятого триплета изомеров, а также от температуры ( в широком интервале), несмотря на то что выход этих продуктов изменяется в этом интервале более чем на порядок. Распределение различных групп углеродных атомов дает их относительная концентрация вместе с соответствующей концентрацией гексильных радикалов. Распределение позволяет оценить, в каком соотношении эти радикалы исчезают путем диспропорционирования и в какой степени димерные продукты образуются соединением радикалов. [41]
Страницы: 1 2 3