Отрицательный заряд - анион
Cтраница 1
Отрицательный заряд аниона будет равномерно распределен между этими атомами кислорода. Были высказаны различные точки зрения на то, почему распределение заряда стабилизует ион и, следовательно, усиливает кислоту. Одно из объяснений основано на электростатической модели. Другой подход базируется на квантовой теории и объясняет стабилизацию либо резонансом или мезомерией нескольких структур иона, либо ( что то же самое) понижением энергии - молекулярной орбитали за счет делокализации электронов по нескольким связям. Хотя квантовый подход должен быть более фундаментальным, однако оценить его пригодность для обсуждаемой проблемы довольно трудно, так как применение этого подхода зависит отточки зрения на природу связей X-О в молекуле кислоты и в анионе. [1]
Отрицательный заряд аниона не сосредоточен целиком на атоме кислорода. [2]
Отрицательный заряд аниона концентрируется на внешней электронной оболочке. Строение катион подходят друг к другу на конечное рас - NaF с позиций тео-стояние и между ними возникает силовое элек - рии Косселя ( соот-трическое поле, тем большей напряженности, ношения в размечем больше заряд этих ионов. Основная часть сунке нНе переданРы) силовых линий такого поля направлена вдоль образующих конуса, в вершине которого находится катион, а в основании - анион. Чем меньше размеры аниона, тем более вытянут конус. [3]
Отрицательный заряд аниона, безусловно, распределен между двумя электроотрицательными атомами, вследствие чего анион может алкилироваться под действием диалкилсульфатов или галогенпроизвбдных с образованием как 0 -, так и N-производных ( ср. Некоторые оксимы, особенно 1 2-диоксимы, могут давать комплексы с катионами переходных металлов. Оксимы также легко ацилируются при действии хлорангидридов или ангидридов кислот, но аль-доксимы склонны при этом дегидратироваться в соответствующие нитрилы. [4]
Величина отрицательного заряда аниона равна числу принятых электронов. [5]
Величина отрицательного заряда аниона ПАВ, определяющая его адсорбируемость на металле, зависит от эффективной электронной плотности на атоме кислорода в сульфогруппе, которая, в свою очередь, определяется суперпозицией индукционных эффектов атомов и их групп, входящих в молекулу. Следовательно, технологические свойства ПАВ в значительной степени определяются строением его молекулы. [6]
Для простоты отрицательный заряд анионов впоследствии опускается. [7]
Таким образом, отрицательный заряд аниона не сосредоточен на центральном метановом атоме, но распределен между ним и девятью углеродными атомами ( всеми о - и n - атомами) бензольных циклов. Конечно, рассредоточение заряда по углеродам играет некоторую ( но только подчиненную) роль и в тринитротрифенилметил-анионе, где заряд в большей части сосредоточен уже на кислородных атомах нитрогрупп. [8]
Таким образом, отрицательный заряд аниона не сосредоточен на центральном метановом атоме, но распределен между ним и девятью углеродными атомами ( всеми о-и га-атомами) бензольных циклов. Конечно, рассредоточение заряда по углеродам играет некоторую ( но только подчиненную) роль и в тринитротрифенилметил-анионе, где заряд в большей части сосредоточен уже на кислородных атомах нитрогрупп. [9]
В результате резонанса отрицательный заряд аниона распределяется по всей молекуле, что намного выгоднее концентрации заряда на одном атоме, как это имело место в алкоксид-анионе. Отсюда следует важный вывод: фенолы - более сильные кислоты, чем спирт. Это объясняется тем, что энергия, необходимая для ионизации фенола, меньше энергии ионизации спирта благодаря хорошей стабилизации феноксид-аниона ( ср. [10]
Этот эффект обусловлен стабилизацией отрицательного заряда аниона более поляризуемыми алкильными группами. В газовой фазе такая стабилизация преобладает над индуктивным эффектом, который в свою очередь проявляется в растворе. [11]
Кч особенностям кислородсодержащих кислот как окислителей относится отрицательный заряд аниона, в котором центральный атом восстанавливается в ходе реакции. Возникает вопрос, могут ли такие анионы реагировать путем простого электронного перехода. Некоторые исследователи считают, что такой переход невозможен и что в действительности кислородная кислота вступает в реакцию в виде нейтральной молекулы. [12]
Заметим, что стабилизация в результате делокализа-ции отрицательного заряда анионов, соответствующих карбоновым кислотам ( IV), фенолам ( V), псевдокислотам ( VI) и триарилметанам ( VII), является причиной кислых свойств каждого из этих соединений. [13]
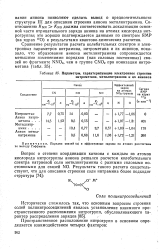 |
Параметры, характеризующие электронное строение нитрометана, метилнитрамина и их анионов. [14] |
Соотношению / CNN KNO должна соответствовать локализация основной части отрицательного заряда аниона на атомах кислорода нит-рогруппы; это хорошо подтверждается данными по спектрам ЯМР ( на ядрах 17О) и результатами квантово-химических расчетов. [15]
Страницы: 1 2 3 4