Отрицательный заряд - анион
Cтраница 2
Вероятно, такая сравнительно высокая кислотность обусловлена значительной делокализацией отрицательного заряда аниона между четырьмя атомами азота, однако алкилирование аниона ( разд. [16]
В этом случае положительный заряд катиона должен быть нейтрализован отрицательным зарядом аниона. Если осаждение проводят в обычных условиях, то этим анионом, без сомнения, должен быть сульфат-ион. Поскольку масса железа, связанного с сульфат-ионом, меньше, чем масса бария, связанного с тем же анионом, осадок будет слишком легким, и результат по сульфату будет занижен. Обычно соосаждение посторонних катионов приводит к заниженным результатам в определении сульфата. [17]
Кислотная диссоциация гидридных комплексов переходных металлов возможна лишь тогда, когда отрицательный заряд аниона ( сопряженного основания), образующегося при отрыве протона, может быть делокализован по нескольким сильным электроноакцепторным лигандам, в особенности СО-группам. Кроме того, обращению полярности связи М - Н может способствовать энергетический выигрыш сольватации протона в водных или спиртовых растворах. Пока мы рассмотрели лишь стадию актнаации водорода, а теперь проследим дальше каталитический цикл гидрирования на катализаторе Уилкннсона. [18]
И при диссоциации солей число положительных зарядов катионов всегда равно числу отрицательных зарядов анионов. [19]
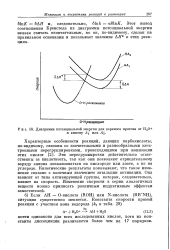 |
Диаграмма потенциальной энергии для переноса протона от Н30. [20] |
Эти перегруппировки действительно ответственны за кислотность, так как они позволяют отрицательному заряду аниона локализоваться на кислороде или азоте, а не на углероде. Кинетические результаты показывают, что такое изменение связано с конечным значением энтальпии активации. Она зависит от типа активирующей группы, которая, следовательно, влияет на скорость. [21]
Причина кислотности водородного атома при тройной связи состоит в том, что отрицательный заряд аниона RC C - эффективно делокализо-ван, благодаря взаимодействию электронной пары с облаком л-электро-нов связи С С. [22]
 |
Константы диссоциации К некоторых слабых электролитов ( при 25 С. [23] |
При ступенчатой диссоциации многоосновных кислот отщепление последующих ионов водорода затрудняется вследствие увеличения отрицательного заряда аниона и энергии связи иона водорода с анионом. Аналогичное явление наблюдается также при диссоциации солей. [24]
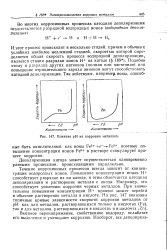 |
Влияние рН на коррозию металлов. [25] |
Подобно этому и разрядка других катионов ( полная или частичная) или повышение отрицательного заряда анионов могут способствовать катодной деполяризации. [26]
Подобно этому и разрядка других катионов ( полная или частичная) или повышение отрицательного заряда анионов могут способствовать катодной деполяризации. Так действуют, например, ионы, способные бытв окислителями, как ионы Fe3 e - - - Fe2, лоэ. Fe в растворе стимулирует процесс коррозии. [27]
Показанная здесь схема уровней относится только к двум наиболее подвижным электронам, которые несут отрицательный заряд аниона. [28]
Пиррол в то же время представляет собой слабую кислоту, сопряженное основание которой стабилизовано делокализацией отрицательного заряда аниона точно так, как фтальимидный анион ( стр. [29]
 |
Поляризационные кривые восстановления иона S20 из раствора КгЯгОз в присутствии разных количеств Na2S04 ( на вращающемся амальгамированном элек. [30] |
Страницы: 1 2 3 4