Производство - перхлорат
Cтраница 1
Производство перхлоратов осуществляют почти исключительно электрохимическим путем. Электролизу подвергают водный раствор хлората натрия. Однако получающийся перхлорат натрия не находит широкого применения вследствие его сильной гигроскопичности и расплывания на воздухе. Обменным разложением его с хлоридами или сульфатами калия или аммония получают перхлорат калия или аммония. [1]
Производство перхлоратов осуществляют почти исключительно электрохимическим путем. Электролизу подвергают водный раствор хлората натрия. Однако получающийся перхлорат натрия не находит широкого применения вследствие его сильной гигроскопичности и рас-плывания - на воздухе. Обменным разложением его с хлоридами или сульфатами калия или аммония получают перхлорат калия или аммония. [2]
В производстве перхлоратов до последнего времени применяли только платиновые или платинотитановые аноды. Аноды с активным слоем из смеси окислов рутения и титана в условиях получения перхлората нестойки, их нельзя применять в этом процессе. [3]
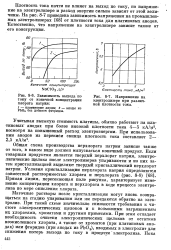 |
Зависимость выхода по току от конечной концентрации хлората натрия. 1 - платиновые аноды. 2 - аноды из PbOj без добавок фторидов.| Напряжение на электролизере при различной плотности тока. [4] |
Общая схема производства перхлората натрия зависит также от того, в каком виде должен выпускаться конечный продукт. Если товарным продуктом является твердый перхлорат натрия, электролитические щелока после электролизеров упариваются и из них затем кристаллизацией выделяют твердый кристаллический перхлорат натрия. Прямая линия, пересекающая поле рисунка, характеризует изменение концентрации хлората и перхлората в ходе процесса электролиза по мере окисления хлората. [5]
 |
Выход по току при различной концентрации ЫаСЮз.| Напряжение на электролизере при различной плотности тока. [6] |
Общая схема производства перхлората натрия зависит также от того, в каком виде должен выпускаться конечный продукт. Если конечным продуктом является твердый перхлорат натрия, электролитические щелока, отбираемые из электролизеров, упаривают, а затем из них путем кристаллизации выделяют твердый кристаллический перхлорат натрия. Прямая линия, пересекающая поле рисунка, показывает изменение концентрации хлората в процессе электролиза по мере его окисления. [7]
Технико-экономические показатели производства перхлората натрия зависят частично от количества платины, потерянной в ванне. Разрушение платины происходит вследствие химической коррозии ( преобладающий процесс) и путем эррозии. Платина, разрушаемая в результате коррозии, не обязательно должна находиться в электролите, удаляемом из электролизера в растворенном состоянии; часть ее может содержаться в шламе, выгружаемом из ванны. Можно предположить, что коррозия возникает на гранях кристаллов платины, где наблюдается наибольшая концентрация загрязняющих примесей. Когда материал на гранях химически разрушается, твердые кристаллы платины отделяются и попадают в шлам. [8]
Завод по производству перхлоратов был построен в 1893 г. в Мансбо ( Швеция); в 1898 г. удалось получить небольшие количества перхлората аммония, причем режим производства еще не-был отработан. Так, в одном случае ванна раствора хлората натрия окислялась до перхлората в течение 5 - 6 Дней, а в другом - процесс затягивался на многие недели. К 1904 г. производство уже было налажено. [9]
Завод по производству перхлоратов был построен в 1893 г. в Мансбо ( Швеция); в 1898 г. удалось получить небольшие количества перхлората аммония, причем режим производства еще не-был отработан. Так, в одном случае ванна раствора хлората натрия окислялась до перхлората в течение 5 - 6 Дней, а в другом - процесс затягивался на многие недели. К 1904 г. производство уже было налажено. [10]
Поскольку основным методом производства перхлоратов является электрохимический, рассмотрим некоторые его особенности. [11]
Содержится в выбросах производств перхлоратов, реактивов аналитической химии, катализаторов гидролиза и этерификации гальванических. [12]
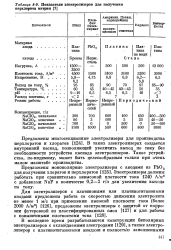 |
Показатели электролизеров для получения перхлората натрия. [13] |
Предложены многосекционные электролизеры для производства перхлоратов и хлоратов [,124], В таких электролизерах создается внутренний каскад, позволяющий увеличить выход по току без необходимости устройства каскада электролизеров. Такое устройство, по-видимому, может быть целесообразным только при очень малом масштабе производства. [14]
Последнее положило начало развитию производства перхлоратов во время первой мировой войны. Так, в Германии за годы войны было выработано около 20 тыс. т перхлоратов [5], а мировое производство. После окончания войны производство перхлоратов резко сократилось и получило новое развитие только в годы второй мировой войны. [15]
Страницы: 1 2 3