Дибензофурана
Cтраница 1
Дибензофураны обладают более слабым пестицидным действием и практического применения в сельском хозяйстве пока не получили. [1]
Дибензофураны обычно получают дегидратацией 2 2 -дигидр-оксибнфенилов [213, 2.4], разложением соответствующих бисдиазо-ниевых солей, циклизацией о-аминоднфениловых эфиров с помощью диазотирования, а также при дальнейших превращениях бензофуранов. [2]
Дибензофураны обладают более слабым пестицидным действием и практического применения в сельском хозяйстве пока не получили. [3]
Некоторые алкиламиноалкиловые эфиры дибензофуран -, карбазол-и дибензотиофенкарбоновых кислот [78] действуют как очень сильные местные анестезирующие средства; однако эти соединения раздражают кожу, и это препятствует их практическому применению. [4]
ПХБ образуют диоксины и дибензофураны. [5]
При таллировании бензола и дибензофурана необходимо более продолжительное нагревание. [6]
Свидетельств того, что полихлорированные дибензофураны ( ПХДФ) являются селективно иммуннотоксичными для животных, не имеется. Об исследованиях по действию ПХДФ на развивающуюся иммунную систему не сообщалось: но исследования проведенные на взрослых животных указывают на то, что происходит умеренное подавление иммунной системы при дозах, которые являются явно токсичными. [7]
 |
Острая токсичность диоксинов и родственных соединений. [8] |
Кроме того, диоксины, дибензофураны и бифенилы имеют высокую химическую и термическую устойчивость. [9]
Влияние заместителей [20] на образование производных дибензофурана по этому методу было изучено для нитро -, бромнитро - и бромпроизводных диацетата 2 2 -диоксидифенила. Установлено, что введение нитрогруппы в орто - или пара-положение по отношению к ацилированным оксигруппам облегчает образование цикла тогда как нитрогруппа, находящаяся в мета-положении, препятствует циклизации. Введение брома в диацетат диокси-дифенила препятствует удалению ацетоксигрупп и образованию цикла. [10]
Здесь мы ограничимся рассмотрением фурана, бензофурана, дибензофурана и тиофена. [11]
Вполне устойчивы, например, анион-радикалы 1-изопропилкарбазола, дибензофурана и ди-бензотиофена. [12]
При обработке дигидродибензофурана w - Na-бутилом получается 66 % дибензофурана и 21 6 % дибензофуран-4 - карбоновой кислоты. При этом образуется до 34 % соответствующей кислоты. Окислением бромом в растворе уксусной кислоты она может быть превращена в дибензофуранкарбоновую кислоту. [13]
К раствору 42 г ( 0 25 моля) дибензофурана в 150 мл абсолютного эфира прибавляют раствор 0 4 моля - бутиллития в эфире. Полученный раствор перемешивают при комнатной температуре в течение 38 час. Не прекращая перемешивания, к реакционной смеси очень медленно приливают раствор 6 1 г ( 0 13 моля) метоксиамина в 40 мл абсолютного эфира. После этого баню отставляют; смесь перемешивают в течение еще 2 час. Эфирный слой отделяют; водный слой дважды экстрагируют эфиром, после чего соединенные эфирные растворы сушат над сернокислым натрием. Раствор фильтруют, чтобы освободить от следов дибензофурана, и фильтрат подщелачивают добавлением водного раствора аммиака. [14]
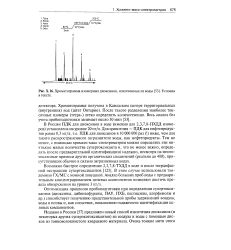 |
Хроматограмма изомерных диоксинов, извлеченных из воды. Условия в тексте. [15] |
Страницы: 1 2 3 4