Протеиназа
Cтраница 3
Прямоугольники - экзоны; треугольники - положение нитронов; а - ген активатора плазминогена ( сериновой протеиназы) / - палец фнбронектииа; / / - гомология с экзоном эпидермальиого фактора роста; / / / - экзоны протеазного домена; б - ген рецептора липо - Протенда низкой плотности: / - сигнальная последовательность; / / - домен, связывающий липопротеид ( гомология с экзоном в гене фактора комплемента С9 указана штрихами. [31]
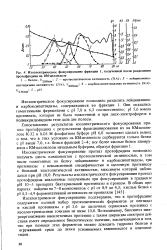 |
Изоэлектрическое фокусирование фракции 1, полученной после разделения протофрадина на КМ-целлюлозе. [32] |
Результаты изоэлектрического фокусирования протеаз протофрадина аналогичны полученным при фокусировании в градиенте рН 10 - 3 препарата бактериальной протеиназы и проназы. [33]
Еще один механизм регуляции активности автолизинов сопряжен с их инактивацией протеиназами, в которой доминирующую роль отводят сериновым протеиназам. Специфические природные ингибиторы сериновых протеиназ, в частности низкомолекулярный пептид MAPI, регулируя активность протеолиза, вторично влияют на функциональность автолизинов. [34]
В заключение хотелось бы отметить, что настоящий обзор является первой попыткой обобщения имеющихся в литературе данных о внеклеточных протеиназах актиномицетов. Из содержащегося в обзоре материала отчетливо видно, как невелики наши познания в этой области и как недостаточны они для характеристики получаемых препаратов. Сравнительная оценка свойств препаратов практически невозможна, так как в большинстве случаев мы располагаем только единичными фактами и данными. [35]
С помощью протеолитических ферментов получ ают различные белковые гидролизаты молока, расщепляя в нем белки папаином, бромелином, протеиназами грибов или бактерий. Вырабатывают, например, легко усвояемые молочные продукты для больных или детей. Коровье или козье молоко гидролизуют, нагревая с препаратами протеаз при 50 - 60 С, прибавляя лимоннокислые и фосфорнокислые соли ( Na или К), заменяя на натрий или калий часть содержащегося кальция. Белковые гидролизаты, необходимые для приправ, специальных диет и кормов, получают, проводя глубокий ферментативный протеолиз белков мяса, рыбы или молока. Как и в случае карбогидраз, ферментативное расщепление имеет преимущества перед кислотным или щелочным. Оно технически проще и не вызывает разрушения или рацемизации аминокислот. [36]
Для выяснения положения амидных групп аспарагина и глутамина было проведено дополнительное ферментативное расщепление фракций А и В папаином и плесневой протеиназой. [37]
Очевидным продолжением вышеописанной техники является комбинация газо-жидкостной хроматографии и масс-спектрометрии для того, чтобы разделять и идентифицировать короткие пептиды, получаемые после гидролиза протеиназами. Например, ди-пептиды, получаемые гидролизом с помощью дипептидиламино-пептидазы ( см. разд. [38]
С помощью достаточного количества соляной кислоты в измельченной ткани устанавливается кислотность, при которой происходит быстрое превращение пепсиногена в пепсин и предотвращается разрушение пепсиногена и пепсина другими тканевыми протеиназами. [39]
Полицитидиловая кислота 317 Предшественник белка ( РЭ2) головки бактериофага Т4 357 Прекалликреин 321 Прока: рбоксипептидаза 3 21 Пролактин 337 Пролилгидроксилаза 317 Пропердин 363 Протаминкиназа 310 Протеиназа. [40]
По зависимости активности от концентрации буферных растворов эластаза протоальбина более сходна с одной из эластаз римопротелина ( см. раздел Эластазы) - Можно предполагать, что эта эластолитиче-ская протеиназа по своей специфичности способна гидролизовать эластин, но вследствие того, что она является нейтральной протеиназой, ее способность сорбироваться на эластине выражена не так сильно, как у эластаз проназы, протелина и протофрадина. [41]
Так, например, цианиды ( соли синильной кислоты) почти полностью блокируют дыхательный фермент, но заметно повышают активность папаина ( растительной протеазы), катепсина ( животной протеиназы) и некоторых других ферментов. [42]
Активность грибных и бактериальных протеиназ определяют при следующих значениях рН: 2 5 0 2 - кислая протеиназа; 3 5 0 2 - кислая протеиназа; 7 2 0 2 - нейтральная протеиназа; 9 5 0 2 - щелочная протеиназа. [43]
Активность грибных и бактериальных протеиназ определяют при следующих значениях рН: 2 5 0 2 - кислая протеиназа; 3 5 0 2 - кислая протеиназа; 7 2 0 2 - нейтральная протеиназа; 9 5 0 2 - щелочная протеиназа. [44]
По зависимости активности от концентрации буферных растворов эластаза протоальбина более сходна с одной из эластаз римопротелина ( см. раздел Эластазы) - Можно предполагать, что эта эластолитиче-ская протеиназа по своей специфичности способна гидролизовать эластин, но вследствие того, что она является нейтральной протеиназой, ее способность сорбироваться на эластине выражена не так сильно, как у эластаз проназы, протелина и протофрадина. [45]
Страницы: 1 2 3 4