Протеинкиназа
Cтраница 2
Так же как и dsl, эта протеинкиназа находится в неактивном ( латентном) состоянии до тех пор, пока она не вступит во взаимодействие с двуспиральной РНК. Не исключено, что это либо тот же белок, что и dsl, либо dsl входит в состав фермента интерферонобработанных клеток в качестве одной из субъединиц. [16]
Циклические аденинмононуклеотиды в цитоплазме взаимодействуют с ферментом протеинкиназой А или С, которая в отсутствие цАМФ находится в неактивном состоянии. [17]
Показано, что существует спец, Са - калмо-дулинзависимая протеинкиназа ( ЕР-2-киназа), к-рая может активироваться при разл. ЕР-2 в клетке; фосфоршшро-ванный ЕР-2 теряет способность эффективно катализировать транслокацию, и элонгация на всех мРНК замедляется. Фосфатазы или их активация легко обращают этот эффект. [18]
На рис. 9.13 суммированы возможные центры действия системы сАМР - протеинкиназа в синапсе. Эта система может, например, регулировать пресинаптический синтез медиатора. [19]
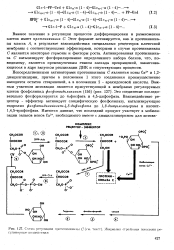 |
Схема регуляции протеинкиназы С ( текст. Жирными стрелками показаны ре-гуляторные воздействия. [20] |
Важное значение в регуляции процессов дифференцировки и размножения клеток имеет протеинкиназа С. Этот фермент активируется, как и протеинкина-зы класса А, в результате взаимодействия специальных рецепторов клеточной мембраны с соответствующими эффекторами, которыми в случае протеинкиназы С являются некоторые гормоны и факторы роста. Активированная протеинкиназа С катализирует фосфорилирование определенного набора белков, что, по-видимому, является промежуточным этапом каскада превращений, заканчивающегося в ядре запуском репликации ДНК и сопутствующих процессов. [21]
Получены доказательства, что большинство эффектов цГМФ опосредовано через цГМФ - зависимую протеинкиназу, названную протеинкина-зой G. Этот широко распространенный в эукариотических клетках фермент получен в чистом виде ( мол. [22]
 |
Ковалентная регуляция гликогенфосфорилазы. [23] |
Под действием киназы фосфорилазы Ь, активность которой регулируется цАМФ - зависимой протеинкиназой, обе субъединицы молекулы неактивной формы фосфорилазы b подвергаются ковалентному фосфорилиро-ванию и превращаются в активную фосфорилазу а. Дефосфорилирование последней под действием специфической фосфатазы фосфорилазы а приводит к инактивации фермента и возврату в исходное состояние. [24]
Целью работы является получение в частично очищенном состоянии нативного холофермента цАМФ - зависимой протеинкиназы, определение его цАМФ - связывающей активности, изучение способности диссоциировать под действием цАМФ и определение фосфотрансферазной активности свободной С. [25]
Кроме этого, известно, что глюкагон и адреналин через цАМФ - зависи-мую протеинкиназу катализируют фосфорилирование ацетил - КоА - карбокси-лазы и переводят ее в неактивную форму, тем самым ингибируя процессы ли-погенеза. Что касается механизма регуляторного действия СТГ и АКТГ, также активирующих процессы липолиза, то первичный механизм их действия связан, по-видимому, с индукцией синтеза аденилатциклазы и гормончувстви-тельной липазы. Здесь уместно напомнить, что если адреналин стимулирует липолиз почти мгновенно, то действие гормонов гипофиза на липолиз характеризуется наличием достаточно продолжительной лаг-фазы. [26]
Рапамицин также связывается с иммунофилинами, но его мишенью является не кальциневрин, а протеинкиназа, участвующая в механизмах синтеза а-цепи рецептора для IL-2. В результате способность к синтезу этого рецептора ингибируется, а клетка теряет способность к активации. [27]
 |
Схема активации фосфорилазы. [28] |
Имеется семейство цГМФ - зависимых протеинкиназ ( протеинкиназы G), которые осуществляют фосфорилирование белков, подобно протеинкиназам А или С. [29]
Из представленных ниже компонентов составьте схему процесса, активность которого возрастает в жировой ткани при интенсивной физической нагрузке: 1) протеинкиназа неактивная; 2) протеинкиназа активная; 3) триацилглицеринли-паза нефосфорилированная; 4) триацилглицеринлипаза фос-форшшрованная; 5) аденилатциклаза неактивная; 6) адени-латциклаза активная; 7) ТцАМФ; 8) АТФ; 9) адреналин. [30]
Страницы: 1 2 3 4 5