Протеинкиназа
Cтраница 3
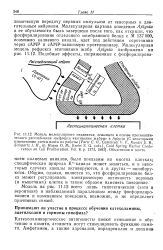
Из представленных ниже компонентов составьте схему процесса, активность которого возрастает в жировой ткани при интенсивной физической нагрузке: 1) протеинкиназа неактивная; 2) протеинкиназа активная; 3) триацилглицеринли-паза нефосфорилированная; 4) триацилглицеринлипаза фос-форшшрованная; 5) аденилатциклаза неактивная; 6) адени-латциклаза активная; 7) ТцАМФ; 8) АТФ; 9) адреналин. [31]
Киназа фосфорилазы-это очень крупный белок с молекулярной массой свыше 1 млн. Она состоит из 16 субъединиц, каждая из которых содержит специфический остаток серина, который под действием активированной протеинкиназы фосфорилируется посредством АТР. [32]
В 1978 году был открыт первый онкоген, привносимый в клетки человека и животных ретровирусом: оказалось, что белок, кодируемый этим вирусом ( онкобелок), является ферментом протеинкиназой и способен превращать нормальную клетку в опухолевую. Затем выяснилось, что в нормальных клетках различных видов животных и человека содержатся белки, идентичные онкобелкам. Соответствующие гены были названы клеточными онкогенами. [33]
Молекулярная картина поведения Aplysia и ее обучаемости была завершена после того, как открыли, что фосфорилирование отдельного мембранного белка с М 137000, возможно калиевого канала, идет под действием серотонина через сАМР и сАМР - зависимую протеинкиназу. [35]
Про те инки на за - это внутриклеточный фермент, через который цАМФ реализует свой эффект. Протеинкиназа может существовать в 2 формах. В отсутствие цАМФ Протеинкиназа представлена в виде тетрамерного комплекса, состоящего из двух каталитических ( С2) и двух регуляторных ( Rj) субъединиц с мол. В присутствии цАМФ протеинкиназный комплекс обратимо диссоциирует на одну К2 - субъединицу и две свободные каталитические субъединицы С; последние обладают ферментативной активностью, катализируя фосфорилирование белков и ферментов, соответственно изменяя клеточную активность. [36]
Далее сАМР связывается с регу-ляторной субъединицей протеинкиназы, что вызывает высвобождение каталитической субъединицы и тем самым ее активацию. Протеинкиназа фосфорилирует неактивную киназу фосфорилазы, которая на следующем этапе стимулирует гликоген-фосфорилазу. [37]
АМФ оказывает влияние и на дефосфорилирование белков, к-рое осуществляется под действием протеинфосфатаз. Так, Протеинкиназа фосфорилирует один из белков, в результате чего он приобретает св-ва ингибировать фосфата-зу 1 - фермент, катализирующий дефосфорилирование. Метаболизм цАМФ осуществляют два фермента - аденил-атциклаза, катализирующая синтез цАМФ из АТФ, и фосфодиэстераза цАМФ, к-рая катализирует гидролиз цАМФ по З - фосфоэфирной связи с образованием 5 -адено-зинмонофосфата. [38]
Протеинкиназа С в условиях повышенной концентрации Са в цито-золе клетки имеет очень важные и разнообразные функции. В данном случае активированная протеинкиназа С способствует перемещению белков цитоскелета в направлении активированного рецептора. Этому процессу благоприятствует и повышение концентрации Са со стороны такого рецептора. [39]
Процесс дефосфорилирования белков происходит под действием ферментов группы фосфопротеинфосфатаз. Фосфорилирование белков цАМФ - зави-симыми протеинкиназами не ограничивается цитоплазмой. С-Каталитиче - ские субъединицы протеинкиназ способны пересекать ядерные мембраны и, фосфорилируя ядерные белки - гистоны, регулировать генную активность клеток. [40]
Основное различие между двумя этими типами заключается в способности регуляторных субъединиц киназ типа II фосфорилироваться каталитической субъединицей. В то же время cGMP - зависимая протеинкиназа представляет собой димерный белок, состоящий из двух идентичных субъединиц. [41]
Новые данные свидетельствуют о том, что в клетках фосфопротеины синтезируются в результате посттрансляционной модификации, подвергаясь фосфорилированию при участии протеинкиназ. Здесь лишь укажем на существенную роль специфической протеинкиназы, катализирующей фосфорилирование ОН-группы тирозина, в биосинтезе онкобелков. Следует отметить, что фосфопротеины содержат органически связанный, лабильный фосфат, абсолютно необходимый для выполнения клеткой ряда биологических функций. Кроме того, они являются ценным источником энергетического и пластического материала в процессе эмбриогенеза и дальнейшего постна-тального роста и развития организма. [42]
Такой детальный анализ всей цепи событий оказался возможным благодаря крупным размерам нейронов ( порядка 100 мкм), которые легко идентифицировать, что позволяет вводить в клетку микрозлеироды и производить внутриклеточные инъекции. Например, роль фосфорилярования, осуществляемого протеинкиназой, была установлена путем прямой инъекции протеин-киназы в сенсорный нейрон; наступавшая при этом сенситизация была неотличима от сенситизации, вызываемой раздражением облегчающих нейронов. [43]
 |
Биосинтез катехоламинов. [44] |
Помимо такого аллостерического контроля, для нее обнаружена регуляция посредством фосфори-лирования и дефосфорилирования как в надпочечниках, так и в различных областях мозга. В таком регулировании, очевидно, принимает участие сАМР - зависимая протеинкиназа. В результате фосфорилирования понижается Km для кофактора птери-дина и уменьшается сродство к ингибитору обратной связи, а следовательно, происходит активация фермента. Фосфорили-рование включается при функциональной активности нейронов. [45]
Страницы: 1 2 3 4 5