Протеинкиназа
Cтраница 4
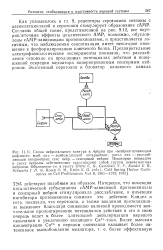
Согласно общей схеме, представленной на рис. 9.12, все внутриклеточные эффекты циклического AMP, возможно, обусловлены сАМР - зависимыми протеинкиназами, и представляется логичным, что наблюдаемая сенситизация имеет некоторое отношение к фосфорилированию ключевого белка. Предварительные электрофизиологические эксперименты показали, что расслабление основано на продленных потенциалах действия и повышенной секреции медиатора иннервированным сенсорным нейроном. [47]
Установлено, что эта киназа может существовать как в активной, так и в неактивной форме. Неактивная киназа фосфорилазы превращается в активную под влиянием фермента протеинкиназы ( киназа киназы фосфорилазы), и не просто протеинкиназы, а цАМФ - зависимой протеинкиназы. [48]
Таким образом, представленные данные о вторичных мессенджерах свидетельствуют о том, что каждой из этих систем посредников гормонального эффекта соответствует определенный класс протеинкиназ, хотя нельзя исключить возможности существования тесной связи между этими системами. Активность протеинкиназ типа А регулируется цАМФ, протеин-киназы G - цГМФ; Са2 - кальмодулинзависимые протеинкиназы находятся под контролем внутриклеточной [ Са2 ], а протеинкиназа типа С регулируется диацилглицеролом в синергизме со свободным Са2 и кислыми фосфолипидами. Повышение уровня какого-либо вторичного мес-сенджера приводит к активации соответствующего класса протеинкиназ и последующему фосфорилированию их белковых субстратов. В результате меняется не только активность, но и регуляторные и каталитические свойства многих ферментных систем клетки: ионных каналов, внутриклеточных структурных элементов и генетического аппарата. [49]
Неактивная фосфорилаза ( Ь) превращается в активную фосфорилазу ( а) в результате ее фосфорилирования фосфорилаза-6 - киназой. Однако последняя также существует в фосфорилированной ( активной) и нефосфорилированной ( неактивной) формах. Протеинкиназа может фосфорилировать не только фосфо-рилазокиназу, но также многие другие белки, такие как казеин и даже гликогенсинтетазу. Фосфорилирование гликогенсинтетазы инактивирует фермент, и в итоге сАМР не только активирует деградацию гликогена, но также и выключает его синтез. В результате каскадного процесса, описанного выше, эффект малого количества сАМР усиливается, сАМР может осуществлять очень тонкий контроль за процессом деградации гликогена. [50]
В 1968 г. Эдвин Кребс и его коллеги показали, что сАМР - за-виси мая протеинкиназа участвует в стимуляции глпкогенолиза. Связывание сАМР с регуляторными субъединицами вызывает диссоциацию их каталитических субъединиц, и последние, таким образом, активируются. Протеинкиназа, найденная в основном в нервных тканях, так называемая киназа типа II, фактически фосфорилирует свои собственные регуляторные субъединицы; такое автофосфорилирование не наблюдается у протеинкиназы типа I. Однако механизмы их активации одинаковы. [51]
Гормоны глюкагон ( в печени) и адреналин стимулируют аденилатциклазу. В результате в цитозоле увеличивается концентрация цАМФ; цАМФ активирует протеинки-назу. Протеинкиназа фосфорилирует за счет АТФ белки-ферменты, в частности второй фермент из класса протеинкиназ - киназу фос-форилазы. Киназа фосфорилазы из неактивной дефосфорилирован-ной формы переходит в активную фосфорилированную. Активная киназа фосфорилазы за счет АТФ переводит фосфорилазу Ь ( неактивная) в фосфорилазу а, которая катализирует фосфоролитическое расщепление гликогена. Параллельно Протеинкиназа фосфорилирует гликогенсинтазу I, переводя ее в неактивную гликогенсинтазу D, т.е. тормозится синтез гликогена. Каскадный механизм позволяет 1 молекуле гормона привести к образованию 107 - 108 молекул глюкозы. [52]
Важное значение в регуляции процессов дифференцировки и размножения клеток имеет протеинкиназа С. Этот фермент активируется, как и протеинкина-зы класса А, в результате взаимодействия специальных рецепторов клеточной мембраны с соответствующими эффекторами, которыми в случае протеинкиназы С являются некоторые гормоны и факторы роста. Активированная протеинкиназа С катализирует фосфорилирование определенного набора белков, что, по-видимому, является промежуточным этапом каскада превращений, заканчивающегося в ядре запуском репликации ДНК и сопутствующих процессов. [53]
Схема регуляции следующая: гормон связывается с рецептором, что приводит к активации фосфолипазы С. Этот фермент катализирует расщепление мембранного фосфатидилинозитол-4 5-бисфосфата на два вторичных посредника - 1Р3 и диацилглицерол. Диацилглицерол активирует фосфолипидзависимую протеинкиназу С. [54]
Про те инки на за - это внутриклеточный фермент, через который цАМФ реализует свой эффект. Протеинкиназа может существовать в 2 формах. В отсутствие цАМФ Протеинкиназа представлена в виде тетрамерного комплекса, состоящего из двух каталитических ( С2) и двух регуляторных ( Rj) субъединиц с мол. В присутствии цАМФ протеинкиназный комплекс обратимо диссоциирует на одну К2 - субъединицу и две свободные каталитические субъединицы С; последние обладают ферментативной активностью, катализируя фосфорилирование белков и ферментов, соответственно изменяя клеточную активность. [55]
Устойчивость к воздействию вирусов обусловлена активацией интерфе-ронами определенных механизмов клетки, вызывающих синтез некоторых белков. Среди них выделяют два фермента, обладающих особой противовирусной активностью. Первый - это протеинкиназа, фосфорилируюшая a - субъединицу фактора elF - 2, который инициирует трансляцию. В результате происходит его инактивация и тем самым блокируется синтез вирусных белков в клетке. Другой фермент - 2; 5 - олигоаденилатсинтетаза, активирующая эндонуклеазу, которая разрушает вирусную РНК. Известны и некоторые другие механизмы антивирусного действия интерферонов. [56]
Однако после фосфорилирования протеинкиназой ( для данного случая называемой фосфорилазой) димерный фермент ассоциирует в активный тетрамер - фосфорилазу а. Тетрамер катализирует расщепление гликогена, в форме которого сохраняется сахар, в мономерную глюкозу. Следовательно, в ответ на появление эпинефрина ( адреналина) уровень сахара в крови повышается. [57]
 |
Схема регуляции фосфоролизл гликогени. [58] |
Однако направление работы двух конечных регуляторных элементов - киназы и-фосфатазы - в этом случае диаметрально противоположное. Активной формой гликогенсинтазы является ее дефосфорилированная форма. Поэтому в отсутствие каталитически активной протеинкиназы при прочих благоприятных условиях функционирует гликогенсинтаза и в клетках идет синтез гликогена. Наоборот, фосфорилированная форма гликогенсинтазы ферментативно неактивна, поэтому в период действия сигнала, включающего аденилатциклазу и таким путем активирующего протеинкиназу, гликогенсинтаза фосфорилируется и становится неактивной, т.е. синтез гликогена прекращается. Аналогично тому, как это было уже рассмотрено на примере пары фосфофруктокиназа - фруктозо-дифосфатаза, такая система регуляции практически исключает одновременную работу двух противоположно действующих систем - синтеза и фосфоролиза гликогена. [59]
Среди различных путей модификации ферментов в живых организмах, имеющих регуляторное значение, наиболее широко известно и наиболее обстоятельно изучено фосфорилирование гидроксигрупп ферментов, в первую очередь гидрок-сигрупп остатков серина и треонина. Фосфорилирование происходит путем переноса 7 - ф сФата молекулы АТФ на гидроксигруппу и катализируется специальными ферментами, известными под общим названием протеинкиназ. В реакциях, катализируемых протеинкиназами, участвуют два белка - один в качестве катализатора, а другой, в ряде случаев тоже фермент, в качестве фосфорилируемого субстрата. [60]
Страницы: 1 2 3 4 5