Протекание - электрохимический процесс
Cтраница 1
Протекание электрохимического процесса в большой степени зависит от материала, используемого для изготовления анодов и катодов, и состояния поверхности последних. Изменяя электрохимические свойства электродных материалов и поверхности электродов, можно влиять на перенапряжение на электродах и на протекание электрохимического процесса. На ход процесса и его селективность можно также воздействовать, изменяя электродную и объемную плотности тока, температуру процесса в целом или температуру непосредственно на аноде или катоде, состав электролита, величину рН, вводя те или иные добавки в электролит. [1]
Протекание электрохимического процесса сопряжено с обменом заряженными частицами между двумя фазами, у которых происходит перераспределение электрических зарядов и, следовательно, возникает скачок электрического потенциала на границе раздела фаз. Появление скачков потенциалов является следствием стремления всякой системы к термодинамическому равновесию. [2]
Протекание электрохимических процессов во многом зависит т природы металла или окислов активного слоя электрода. [3]
Протекание электрохимических процессов во многом зависит от природы металла или окислов активного слоя электрода. [4]
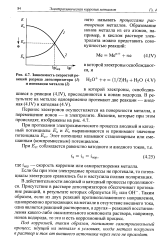 |
Зависимость скоростей реакций разряда деполяризатора ( / НзО 6 ( 1 / 2 Н2 Н. 2О и ионизации металла ( 2. [5] |
При протекании электрохимического процесса анодный и катодный потенциалы Еа и Ек выравниваются и принимают значение потенциала Ест. Этот потенциал называют стационарным или смешанным ( компромиссным) потенциалом. [6]
При протекании электрохимического процесса анодный и катодный потенциалы выравниваются и принимают значение Екор - потенциала коррозии. [7]
При протекании электрохимических процессов происходит перенос электрических зарядов через границу металл-коррозионная среда. В связи с этим скорости окисления металла или восстановление окислителя удобно представлять в единицах силы тока. [8]
 |
Зависимость скоростей реакций разряда деполяризатора ( 7 НзО е ( 1 / 2 Н2 Н2О и ионизации металла ( 2. [9] |
При протекании электрохимического процесса анодный и катодный потенциалы Еа и Ек выравниваются и принимают значение потенциала ЕСТ. Этот потенциал называют стационарным или смешанным ( компромиссным) потенциалом. [10]
В условиях протекания электрохимического процесса, при котором происходит потребление адсорбированного деполяризатора, степень установления адсорбционного равновесия оценивается по ее значению в отсутствие потребления адсорбированного вещества. [11]
Интересная информация о протекании электрохимических процессов может быть получена из переменнотоковых измерений. [12]
Электролитом, необходимым для протекания электрохимического процесса, служит вода с растворенными в ней солями или кислотами и атмосферная вода. [13]
Равномерное капание ртути обеспечивает протекание электрохимического процесса на постоянно обновляющейся, чистой поверхности, состояние которой практически не зависит от предшествовавшей поляризации; поэтому результаты очень хорошо воспроизводятся. [14]
Равномерное капание ртути обеспечивает протекание электрохимического процесса на постоянно обновляющейся, чистой поверхности, состояние которой практически не зависит от предшествовавшей поляризации; поэтому результаты очень хорошо воспроизводятся. [15]
Страницы: 1 2 3 4