Протекание - окислительно-восстановительная реакция
Cтраница 1
Протекание окислительно-восстановительной реакции в данном направлении возможно лишь тогда, когда потенциал восстановления используемого окислителя больше потенциала окисления используемого восстановителя. [1]
Протекание окислительно-восстановительных реакций с участием солей хромовых кислот хорошо наблюдается по изменению окраски растворов от оранжевой до зеленовато-фиолетовой. [2]
Протекание окислительно-восстановительных реакций и, следовательно, изменение степени окисления атомов обусловлено переходом электронов от одних атомов к другим. [3]
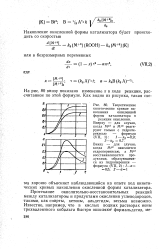 |
Теоретические кинетические кривые накопления окисленной формы катализатора в. [4] |
Протекание окислительно-восстановительных реакций между катализатором и продуктами окисления углеводородов, такими, как спирты, кетоны, альдегиды, весьма возможно. [5]
Протекание побочных окислительно-восстановительных реакций, ведущих к потерям нефтепродукта и кислоты, а также поли-мерообразование в значительной степени регулируют путем поддержания невысокой температуры реакции, которая весьма экзо-термична. Как это ни странно, но потери нефтепродукта с кислым гудроном меньше при температуре очистки 100 С, чем при 25 С. Тем не менее следует избегать слишком высоких температур, поэтому рекомендуется добавлять кислоту к нефтепродукту постепенно, малыми порциями, что обеспечивает относительное постоянство рабочей температуры. [6]
Для протекания окислительно-восстановительной реакции необходимо присутствие веществ, взаимно противоположных по своей способности отдавать или присоединять электроны. Кроме того, известно, что та или иная химическая реакция может протекать только при определенных условиях. Такими условиями чаще всего являются: реакция среды, концентрация участвующих веществ, температура, давление, катализатор, отсутствие или присутствие веществ, мешающих или способствующих протеканию данной реакции. [7]
Обеспечивает протекание окислительно-восстановительных реакций в живых организмах и технологических процессах. [8]
Для протекания окислительно-восстановительных реакций, сопровождающихся образованием свободных радикалов, требуется значительно меньшая энергия активации, чем для реакций термического распада перекисей. [9]
Без протекания электрохимической окислительно-восстановительной реакции по формуле (2.9) и скорость коррозии согласно равенству (2.8) должна быть равна нулю. Это условие приблизительно выполняется у пассивных металлов, поверхностные защитные слои которых являются электрическими изоляторами, например у алюминия и титана. [10]
Возможность протекания окислительно-восстановительных реакций в колонке, ее направление может быть определено с помощью окислительно-восстановительных потенциалов реагирующих веществ. В отличие от окислительно-восстановительных процессов, протекающих в растворе, в колонке по мере движения раствора вдоль колонки местные концентрации реагирующих веществ в зоне невысоки, и исходные вещества, а также продукты реакции уже не оказывают сильного влияния, как в растворе. Ионная сила раствора уменьшается, а величина коэффициентов активности возрастает, приближаясь к единице, поэтому при рассмотрении редокспроцесса, протекающего в колонке, коэффициент активности ионов можно не учитывать. [11]
Возможность протекания окислительно-восстановительных реакций в колонке, ее направление может быть определено с помощью окислительно-восстановительных потенциалов реагирующих веществ. В отличие от окислительно-восстановительных процессов, протекающих в растворе, в колонке по мере движения раствора вдоль колонки местные концентрации реагирующих веществ в зоне невысоки, и исходные вещества, а также продукты реакции уже не оказывают сильного влияния, как в растворе. Ионная сила раствора уменьшается, а величина коэффициентов активности возрастает, приближаясь к единице, поэтому при рассмотрении редокспроцесса, протекающего в колонке, коэффициент активности ионов можно не учитывать. [12]
Направление протекания окислительно-восстановительных реакций во многом определяется реакцией среды. [13]
 |
Стандартные электродные потенциалы в водных растворах при 25 С. [14] |
При протекании окислительно-восстановительных реакций возникает потенциал между восстановленной и окисленной формой вещества. [15]
Страницы: 1 2 3 4