Протекание - окислительно-восстановительная реакция
Cтраница 2
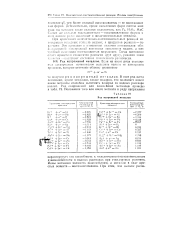 |
Ряд напряжений металлов. [16] |
При протекании окислительно-восстановительных реакций ко иентрацпп исходных веществ падают, а продуктов реакции - во растают. Это приводит к изменению величин потенциалов обе. Когда потенциал обоих процессов становятся равными друг другу, реакция зака. ЧИРлетен - наступает состояние химического равновесия. [17]
При протекании окислительно-восстановительных реакций электроны от вещества-восстановителя переходят к веществу-окислителю. При этом химическая энергия освобождается в виде теплоты. Если же окислитель отделить от восстановителя каким-либо третьим раствором электролита и соединить их между собой металлическим проводником, то тогда реакция восстановления будет протекать на одном конце металлического проводника, реакция окисления - на другом, а электроны, освобождающиеся при реакции окисления, будут перетекать по металлу к окислителю. [18]
При протекании окислительно-восстановительных реакций концентрации исходных веществ падают, а продуктов реакции - возрастают. Это приводит к изменению величин потенциалов обеих полуреакций: электродный потенциал окислителя падает, а электродный потенциал восстановителя возрастает. Когда потенциалы обоих процессов становятся равными друг другу, реакция заканчивается - наступает состояние химического равновесия. [19]
 |
Ряд напряжений металлов. [20] |
При протекании окислительно-восстановительных реакций концентрации исходных веществ падают, а продуктов реакцида - возрастают. Это приводит к изменению величин потенциалов обеих полуреакций: электродный потенциал окислителя падает, а электродный потенциал восстановителя возрастает. Когда потенциалы обоих процессов становятся равными друг другу, реакция заканчивается - наступает состояние химического равновесия. [21]
 |
Ряд напряжений металлов. [22] |
При протекании окислительно-восстановительных реакций концентрации исходных веществ падают, а продуктов реакции - возрастают. Это приводит к изменению величин потенциалов обеих полуреакций: электродный потенциал окислителя падает, а электродный потенциал восстановителя возрастает. Когда потенциалы обоих процессов становятся равными друг другу, реакция заканчивается-наступает состояние химического равновесия. [23]
 |
Ряд напряжений металлов. [24] |
При протекании окислительно-восстановительных реакций концентрации исходных веществ падают, а продуктов реакции - воз растают. Это приводит к изменению величин потенциалов обеих полуреакций: электродный потенциал окислителя падает, а электродный потенциал восстановителя возрастает. Когда потенциалы обоих процессов становятся равными друг другу, реакция заканчивается - наступает состояние химического равновесия. [25]
При протекании окислительно-восстановительных реакций концентрации исходных веществ падают, а продуктов реакции - возрастают. Это приводит к изменению величин потенциалов обеих лолуреакций: электродный потенциал окислителя падает, а электродный потенциал восстановителя возрастает. Когда потенциалы обоих процессов становятся равными друг другу, реакция заканчивается - наступает состояние химического равновесия. [26]
 |
Ряд напряжений металлов. [27] |
При протекании окислительно-восстановительных реакций концентрации исходных веществ падают, а продуктов реакции - возрастают. Это приводит к изменению величин потенциалов обеих полуреакций: электродный потенциал окислителя падает, а эл ек-тродный потенциал восстановителя возрастает. Когда потенциалы обоих процессов становятся равными друг другу, реакция закан-чива. [28]
 |
Ряд напряжений металлов. [29] |
При протекании окислительно-восстановительных реакций концентрации исходных веществ падают, а продуктов реакции - возрастают. Это приводит к изменению величин потенциалов обеих полуреакций: электродный потенциал окислителя падает, а электродный потенциал восстановителя возрастает. Когда потенциалы обоих процессов становятся равными друг другу, реакция заканчивается - наступает состояние химического равновесия. [30]
Страницы: 1 2 3 4