Стационарное протекание - реакция
Cтраница 2
Так как скорость процесса и определяемые ею текущие концентрации компонентов реакции существенно зависят от концентрации промежуточных соединений и, в свою очередь, влияют на них, очевидно, что при стационарном протекании реакции концентрации промежуточных соединений в течение заданного интервала времени не должны изменяться. [16]
В отличие от второй стадии, при пропускании тока ситуация на третьей стадии изменится мало. Поэтому при стационарном протекании реакции процессы на всех быстрых стадиях, в отличие от замедленной, остаются практически равновесными. Применительно к быстрым транспортным стадиям это свидетельствует о сохранении равенства концентраций реагента у поверхности металла и в объеме раствора. [17]
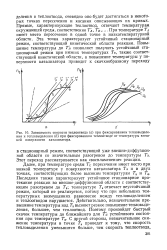 |
Зависимость скорости теплоотвода ( а при фиксированном тепловыделении и тепловыделения ( б при фиксированном теплоотводе от температуры внешней поверхности катализатора. [18] |
Далее, при температуре среды Т с пересечение имеет место при низкой температуре у поверхности катализатора Ti и в двух точках, соответствующих более высоким температурам Ть и Те. Последняя также характеризует устойчивое стационарное протекание реакции во внешне-диффузионной области с соответствующим разогревом до Т6; температуре Тъ отвечает неустойчивый режим, который не реализуется, потому что при небольших температурных возмущениях равновесие между тепловыделением и теплоотводом нарушается. Действительно, незначительное превышение температуры над Т & вызовет резкое повышение тепловыделения, большее, чем теплоотвод. [19]
Изложенное показывает, что стационарное протекание реакции возможно лишь в открытых системах. Только в них при выполнении надлежащих условий состав реакционной смеси ( а следовательно и концентрации промежуточных соединений) может в каждой точке реакционного пространства, в том числе и на катализаторе, сохраняться статистически неизменным во времени. [20]
Стационарная теория теплового взрыва Д. А. Франк-Каменецкого [1, 2], к изложению которой мы сейчас переходим, основана на предположении, что горючая смесь неподвижна, тепловые потоки определяются теплопроводностью реагирующего вещества и пропорциональны градиенту температуры и химическая реакция протекает по объему сосуда неравномерно. Тепловой взрыв в рамках этой теории рассматривается как наступление невозможности существования стационарного протекания реакции в сосуде, при котором тепловыделение полностью компенсируется теплоотводом в стенки. [21]
Рассмотрим этот вопрос подробнее. Цепной вырожденно-разветвлен-ный процесс можно условно разбить на три периода: установление стационарной концентрации свободных радикалов, достижение кинетически-равновесной концентрации промежуточного продукта, инициирующего цепи, и стационарное протекание реакции. [22]
Для теоретического определения области протекания процесса необходимо оценивать скорости процесса диффузии и химической реакции раздельно, как для независимых процессов. Соотношения этих скоростей определяют область протекания процесса в целом. При стационарном протекании реакции термин диффузионная область вовсе не означает, следовательно, что действительная скорость реакции на реакционной поверхности более скорости процесса диффузии к этой поверхности. Благодаря медленности подвода веществ на поверхность, скорость химической реакции на поверхности принудительно становится равной скорости процесса диффузии. Концентрация вещества на поверхности при этом мала, а градиент концентрации около поверхности получается большим. Наоборот, в кинетической области, когда независимо определенная скорость диффузии значительно превышает скорость реакции, равенство скоростей диффузии и реакции наблюдается при мало отличающихся значениях концентраций реагирующих веществ в объеме и на поверхности. [23]
Для теоретического определения области протекания процесса необходимо оценивать скорости диффузии и химической реакции отдельно, как скорости независимых процессов. Отношение определенных таким образом скоростей указывают область протекания процесса в целом. При стационарном протекании реакции термин диффузионная область вовсе не означает, следовательно, что действительная скорость реакции на реакционной поверхности больше скорости диффузии к этой поверхности. Обе эти скорости равны, но благодаря медленному притоку веществ к поверхности скорость химической реакции на поверхности принудительно становится равной скорости диффузии. Концентрация вещества на поверхности при этом мала, а градиент концентрации вблизи поверхности оказывается большим. И наоборот, в кинетической области, где независимо определенная скорость диффузии значительно превышает скорости реакции, равенство скоростей диффузии и реакции наблюдается при мало отличающихся значениях концентраций реагирующих веществ в объеме и на поверхности. [24]
Для теоретического определения области протекания процесса необходимо оценивать скорости диффузии и химической реакции отдельно, как скорость независимых процессов. Отношение определенных таким образом скоростей указывают область протекания процесса в целом. При стационарном протекании реакции термин диффузионная область вовсе не означает, следовательно, что действительная скорость реакции на реакционной поверхности больше скорости диффузии к этой поверхности. Обе эти скорости равны, но благодаря медленному притоку веществ к поверхности скорость химической реакции на поверхности принудительно становится равной скорости диффузии. Концентрация вещества на поверхности при этом мала, а градиент концентрации вблизи поверхности оказывается большим. И, наоборот, в кинетической области, где независимо определенная скорость диффузии значительно превышает скорости реакции, равенство скоростей диффузии и реакции наблюдается при мало отличающихся значениях концентраций реагирующих веществ в объеме и на поверхности. [25]
При таком процессе в каждой точке системы характеризующие его параметры остаются неизменными во времени. Очевидно, что стационарное протекание реакции возможно только в открытых системах. [26]
Рассмотрение базисов маршрутов делает необходимым соотнесение скоростей элементарных стадий и скоростей реакции по каждому маршруту. Учет стехиометрических чисел стадий позволяет уточнить вопрос о соотношении скорости стадии и скорости реакции. В предыдущей главе указывалось, что при стационарном протекании реакции суммарные скорости всех стадий ( за исключением мгновенных) должны быть приблизительно равны. Эта приблизительность связана также с тем, что при однократном химическом превращении в данной системе каждая стадия должна повториться соответственно ее стехиометрическому числу. [27]
Пусть некоторый объем горючей газовой смеси заключен в сосуд, стенки которого нагреты до определенной температуры. Если теплоотвод через стенки сосуда превышает тепловыделение в результате медленной реакции, то смесь не будет разогреваться. Предельным случаем стационарного протекания реакции является равенство количеств тепла, выделяющегося и отводимого в единицу времени. В этом случае процесс становится нестационарным ( саморазгоняющимся) и происходит самовоспламенение смеси. [28]
Продолжительность первого периода равна ( keWQ) и при очень малых W0 может составить несколько часов. Мощное кратковременное инициирование цепей в начале реакции ( большие W0) позволяет практически мгновенно ( за доли секунды) достигнуть стационарной концентрации свободных радикалов. Скорость накопления промежуточного продукта ( и продолжительность второго периода) также зависит от W0, так что искус - СжЕенное инициирование цепей позволяет сократить и второй период реакции. В период стационарного протекания реакции искусственное инициирование, как правило, нецелесообразно, так как на этом этапе реакция сама обеспечивает высокую скорость инициирования цепей за счет промежуточных продуктов. Однако в некоторых случаях дополнительное инициирование оказывается полезным в течение всего хода реакции. Дополнительное инициирование повышает [ Р ] р, а следовательно, и общую скорость реакции. [29]
Продолжительность первого периода равна ( keW0) - 4 и при очень малых W0 может составить несколько часов. Мощное кратковременное инициирование цепей в начале реакции ( большие W0) позволяет практически мгновенно ( за доли секунды) достигнуть стационарной концентрации свободных радикалов. Скорость накопления промежуточного продукта ( и продолжительность второго периода) также зависит от W0, так что искус-с венное инициирование цепей позволяет сократить и второй период реакции. В период стационарного протекания реакции искусственное инициирование, как правило, нецелесообразно, так как на этом этапе реакция сама обеспечивает высокую скорость инициирования цепей за счет промежуточных продуктов. Однако в некоторых случаях дополнительное инициирование оказывается полезным в течение всего хода реакции. Дополнительное инициирование повышает [ Р ] р, а следовательно, и общую скорость реакции. [30]
Страницы: 1 2 3