Протон - группа
Cтраница 2
Величина химического сдвига протона гидроксилыюй группы сильно зависит от полярности связи О - Н, а также от степени ассоциации. Пик молекулярного иона в масс-спектрах спиртов имеет малую интенсивность. Его распад связан с элиминированием молекулы воды и расцеплением связи С-СОН. Молекулярный пик фенолов, как правило, более интенсивен. [16]
Эти сигналы соответствуют протонам метилено-вой группы С-21, которые неэквивалентны вследствие ограни - - ченного вращения вокруг связи 20 - 21; константа геминального взаимодействия равна - 17 6 гц. [17]
Спии-спиновое взаимодействие между протонами метильиых групп мало и ведет только к уширению линий. [18]
В то время как протоны группы Б мало подвержены влиянию растворителя, химический сдвиг протонов группы А заметно изменяется, так что разность сдвигов может стать довольно заметной ( спектр 1), что упрощает определение констант спин-спиновой связи между ядрами ( гл. III), либо уменьшится до нуля. [19]
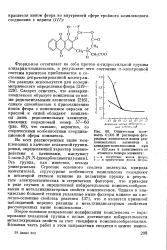 |
Оптическая плотность 0 002 М растворов фто-ридных комплексов ионов редкоземельных элементов с ализарин-комплексоном при А, 622 ммк в зависимости от атомного номера элемента. [20] |
Фторид-ион оттягивает на себя протон а-гидроксильной группы ализарин-комплексона, в результате чего состояние л - электронной системы красителя приближается к состоянию депротонированной молекулы. Следует отметить, что ализарин-комплексон образует комплексы со всеми редкоземельными элементами [216], однако способностью к присоединению ионов фтора с изменением окраски от красной к синей обладают комплексы лишь редкоземельных элементов, имеющих порядковый номер 57 - 60 ( рис. 68), что связано, вероятно, со стерическими особенностями координационной сферы комплекса. [21]
Значение химического сдвига сигнала протона группы NH в аминах колеблется в интервале б 0 5 - 5 0; положение этого сигнала в значительной степени зависит от природы растворителя, концентрации и температуры, поскольку эти факторы влияют на образование межмолекулярных водородных связей. Вследствие этого точное значение химического сдвига протона аминогруппы в указанном интервале имеет очень ограниченное значение для идентификации. Интегрирование спектра позволяет обнаружить исчезновение резонансного сигнала NH, даже если этот сигнал не был разрешен в сложной картине спектра. Сигналы группы NH, как правило, бывают уширенными из-за влияния квадрупольного момента ядер 14N, способствующего более быстрой спин-решеточной релаксации. [22]
Аналогичная зависимость ан с протоном группы С ( 7 - Н от размера заместителя R наблюдается в радикалах XXVIII. Подробнее радикалы XXVI-XXVIII обсуждаются в гл. [23]
При распаде перекиси бензоилпропнонила поляризация протонов групп СН2 и СН3 в продукте рекомбинации PhCO2CH2CH3 противоположна по знаку ( рис. 11.35); она создается в радикальной паре PhC02 CH2CH3 S. [24]
ВС слабо влияет на КССВ протонов группы - АН с ядрами X и другими протонами молекулы. [25]
Хб обнаружен слабо расщепленный дублет протонов нитрометильной группы с химическим сдвигом 6сн2ш2 5 52 и константой спин-спинового взаимодействия / сн2 - Рм 109 гц. [26]
Между сигналами ароматических протонов и протонов алкилышх групп был обнаружен отсутствующий в непротони-рованном углеводороде пик в виде хорошо разрешетюго квадруплета, в то время как пик протонов метильной группы расщепился на дублет. Этот факт свидетельствует о присоединении к атому С-9 протона, который вступает в спин-спиновое взаимодействие с протонами метильной группы, связанной с этим же атомом углерода. [27]
 |
Константы СТВ ( в э в радикалах с сн - конфигурацией. [28] |
Наибольший интерес представляет СТВ с протонами групп R. Очевидно, что на атоме углерода, к которому присоединены группы R, имеется отрицательная я-электронная спиновая плотность. В алифатических цепях наблюдается альтернирование знаков констант СТВ. [29]
Образование водородной связи заключается во взаимодействии протона группы ХН с электронной оболочкой атома-акцептора протона и возмущении электронных оболочек атомов X и Y. Это взаимодействие сказывается особенно отчетливо на изменении волнового числа v и интенсивности / полосы группы ХН. На этой группе, ввиду локального характера водородной связи и отсутствия у протона внутренней электронной оболочки, влияние окружения сказывается меньше, чем на других группах, и потому особенности водородной связи могут наблюдаться в более чистом виде. [30]
Страницы: 1 2 3 4