Гидратированный протон
Cтраница 1
Гидратированный протон, по мнению авторов, присоединяется либо к карбонильной группе, либо к двум атомам кислорода молекулы сложного эфира. [1]
Активность гидратированных протонов представляет собой количественную меру кислотности раствора; ее можно определить с высокой точностью электрохимическими методами. Другое преимущество этой концепции заключается в том, что все процессы - ионизация, нейтрализация и гидролиз соединений ( или более общее - сольво-лиз) - рассматриваются как протолитические реакции. [2]
Эф не зависит от концентрации гидратированных протонов в растворе; в концентрированных растворах серной кислоты образуется нереакционноспо-собная о-протонированная форма амида, что приводит к снижению & Эф реакции циклизации. [3]
И считать, что символ Н обозначает гидратированный протон. [4]
Наиболее распространенные катодные реагенты в естественной среде - это гидратированный протон НзО ( или молекула воды) и растворенный кислород, который постоянно присутствует там, где водная среда находится в контакте с атмосферой. [5]
Данное сообщение имеет целью обсуждение термодинамической устойчивости различных форм гидратированных протонов путем расчета их свободных теплосодержаний гидратации AZ и сопоставления их с опытной величиной. Опытной величиной свободного AZon теплосодержания гидратации мы называем величину, полученную из термохимических опытных данных при помощи соотношения AZ АН - Т AS. [6]
Верхняя строка представляет собой уравнение для катодной поляризации: Н гвдр обозначает гидратированный протон, Ме ( е) - отрицательно заряженную металлическую поверхность ( электрода или порошка); Н - Me - хемосорбированный водород; Н газ - протон в газе, е - свободный электрон, Н - свободный атом водорода, Me - чистую поверхность металла. [7]
При этом имеется в виду, что донором протонов могут быть как гидратированные протоны, так и недиссоциированные молекулы кислоты. [8]
Величина & Ист2 может либо включать константу равновесия образования комплекса реагента с гидратированным протоном, либо не включать, если реакция происходит при соударении. [9]
Последняя реакция показывает взаимодействие между протонами и полярными молекулами воды; формула Н3О соответствует гидратированному протону или иону оксония. [10]
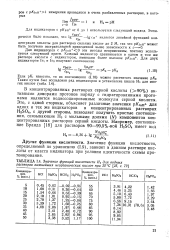 |
Значение функций кислотности Нй для водных растворов важнейших неорганических кислот при 25 С [ 25, с. 79 ]. [11] |
В концентрированных растворах серной кислоты ( 90 %) активными донорами протонов наряду с гидратированными протонами являются недиссоциированные молекулы серной кислоты. Это, с одной стороны, объясняет различные значения р / Сшн для одних и тех же индикаторов в концентрированных растворах H2SO4, с другой стороны, позволяет получить простые соотношения, связывающие Н0 с мольными долями ( N) компонентов концентрированных растворов серной кислоты. [12]
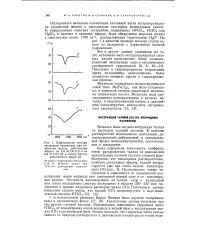 |
Инфракрасные спектры экстрактов, полученных при извлечении железа дибутиловым эфиром из 9 8 М НС Ц / и из 8 2 М LiCl ( 2 и спектр чистого дибутилового эфира ( 3. [13] |
Поскольку в гидратированном гидроксоний заряд, по-видимому, делокализован, более правильно говорить просто о гидратированном протоне. [14]
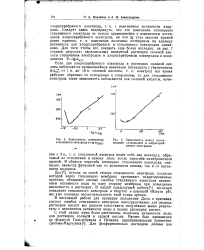 |
Зависимость потенциала стеклянного электрода от lg mHSO.| Зависимость между потенциалами стеклянного и хлоросеребряного электродов. [15] |
Страницы: 1 2 3 4