Протонизация
Cтраница 1
Протонизация А или В облегчает их разряд на электроде. Особенность реакции в том, что она протекает в некотором объеме реакционного слоя вблизи электродной поверхности. Толщина этого слоя ц равна расстоянию, которое может преодолеть электрохимически активная частица АН или ВН за время своего существования. [1]
Протонизации RNCO практически не будет. [2]
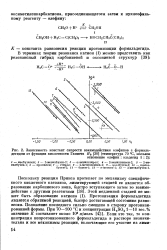 |
Зависимость констант скорости взаимодействия олефинов с формальдегидом от функции кислотности Гаммета Я0 ( температура 70 РС, мольное. [3] |
Протонизация формальдегида является обратимой реакцией, быстро достигающей состояния равновесия. Положение последнего сильно смещено в сторону протонизи-рованной формы. При 70 - 100 С и концентрации H2S04 1 - 10 вес. [4]
Протонизация многокислотных оснований также происходит ступенчато. [5]
Протонизация атома азота, которая вначале кажется предпочтительной, ведет только к образованию исходных веществ. [6]
Последовательная протонизация нормальных комплексов при понижении рН среды может быть показана на примере комплексонатов Mg с нитрилотриметилфосфоновой кислотой. В ИК-спектре раствора нормального комплексоната [ MgL ] 4 - имеет место повышение частот симметричных валентных колебаний vC - Н примерно на 50 см-1 по сравнению с полностью депротонированным, свободным лигандом. Это связано с образованием прочной ковалентной связи Mg - N. Присоединение второго протона происходит к О одной из фосфоновых групп, что проявляется в спектре в виде полосы РО3Н с характерной частотой 1164 см-1. Все эти выводы подтверждаются и спектрами Н и 31Р - ЯМР. [7]
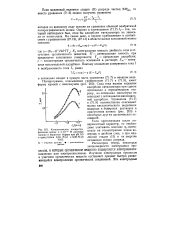 |
Каталитические полярографические волны вЗ - 10 - 6 М растворе хинина в боратном буфере при рН 9 5 в присутствии 0 04 М ( / и 0 06 М ( 2. [8] |
Если протонизация носит поверхностный характер, то необходимо учитывать влияние % - потен-циала на концентрацию ионов водорода в двойном слое, а при медленной стадии ( II) и на энергию активации стадии разряда. [9]
Хотя протонизация карбонила представляет собой существенный фактор при соединении двух структур, но кислотность среды не должна быть слишком большой, чтобы не происходило образования четвертичных аммониевых производных и реакция не утрачивала бы таким образом своего нуклеофильного характера. [10]
При протонизации и образовании солей строение молекулы амина становится близким к тетраэдрическому. [11]
Хотя протонизации во фтористом водороде подвергаются очень многие соединения, число типичных солей весьма ограничено. Те соединения, которые в воде ведут себя как соли, в жидком фтористом водороде подвергаются сольволизу. [12]
Ее протонизация разрушает водородные связи в составном нуклео-филе ( рис. 32), что приводит к потере ферментом каталитической способности. [13]
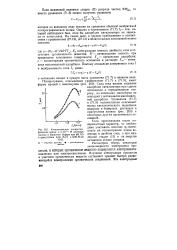 |
Каталитические полярографические волны вЗ - 10 - 6 М растворе хинина в боратном буфере при рН 9 5 в присутствии 0 04 М ( / и 0 06 М ( 2. [14] |
Если протонизация носит поверхностный характер, то необходимо учитывать влияние % - потен-циала на концентрацию ионов водорода в двойном слое, а при медленной стадии ( II) и на энергию активации стадии разряда. [15]
Страницы: 1 2 3 4