Протонизация
Cтраница 3
Процесс его протонизации является обратимым и быстро устанавливающимся сравнительно со скоростью лимитирующего акта реакции. Реакция протекает только через протояи-зоваяйые формы молекул, в отсутствие последних исходное соединение не претерпевает превращения в кислой среде. [31]
Поскольку такая протонизация представляет собой первую стадию аномального гидролиза, становится понятной неспособность S-алкилтиоуксусных кислот к аналогичному превращению. [32]
Если же протонизация не успевает совершиться достаточно быстро, то в данной области потенциалов на полярограмме появляется одноэлектронная волна, и лишь при более отрицательных потенциалах возникает волна, соответствующая второй стадии. [33]
Так как протонизация азо - и аминогрупп описывается разными функциями кислотности [233], при увеличении концентрации кислоты в растворе равновесие I fc II сдвигается в сторону II. Двухзарядные катионы при используемых кислотностях в растворе отсутствуют. [35]
Константы скорости протонизации и обратной реакции - де-протонизации - слабых кислот могут быть определены поляро-графически и по волнам разряда ионов водорода, образующихся в небуферных растворах в приэлектродном пространстве в результате диссоциации молекул слабых кислот. В этой работе была сделана попытка использовать частично ограниченные скоростью диссоциации волны разряда ионов водорода в растворах ряда слабых кислот для определения констант скорости их диссоциации. Однако в полученных в работе [168] уравнениях не был правильно раскрыт физический смысл коэффициента, который соответствует толщине реакционного слоя в теории Брдички - Визнера и, кроме того, для эксперимента были выбраны слишком сильные кислоты [169], поэтому в работе [168] не удалось определить численных значений констант скорости диссоциации. [36]
В степени протонизации важную роль играет стабилизация аниона. [37]
Роль процесса протонизации отчетливо проявляется также при электровосстановлении ароматических кетонов. Последние в кислых растворах образуют две отчетливые одноэлектронные полярографические волны, которые в нейтральной среде сливаются в одну двухэлектронную волну. Первая полярографическая волна, как установлено, отвечает восстановлению протонирован-ной формы кетона до свободного радикала. [38]
Константы скорости протонизации и обратной реакции - де-протонизации - слабых кислот могут быть определены поляро-графически и по волнам разряда ионов водорода, образующихся в небуферных растворах в приэлектродном пространстве в результате диссоциации молекул слабых кислот. В этой работе была сделана попытка использовать частично ограниченные скоростью диссоциации волны разряда ионов водорода в растворах ряда слабых кислот для определения констант скорости их диссоциации. Однако в полученных в работе [168] уравнениях не был правильно раскрыт физический смысл коэффициента, который соответствует толщине реакционного слоя в теории Брдички - Визнера и, кроме того, для эксперимента были выбраны слишком сильные кислоты [169], поэтому в работе [168] не удалось определить численных значений констант скорости диссоциации. [39]
Детальное изучение протонизации замещенных анилинов в уксусной кислоте позволяет определить вклады К. [40]
 |
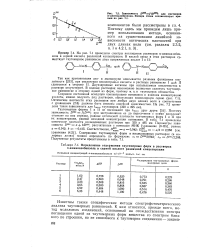
Зависимость р-константы скорости протонизации дианионов. [41] |
При изучении протонизации дианионов малеиновой кислоты почти все буферные растворы содержали лишь по одному кислотному компоненту ( не считая ионов водорода и воды), т е были составлены из соли только одной кислоты. [42]
В случае поверхностной предшествующей протонизации ЕЧ, с ростом рН также становятся отрицательнее. Однако зависимость ЕЧ, от рН несколько сложнее, чем это дает уравнение ( 5), так как, во-первых, в известной мере изменяется [18] с рН значение bb l ( b - 6), во-вторых, рН в приэлектродном слое и в глубине раствора различны и, в-третьих, в скобках правой части уравнения ( 2) помимо первого члена от рН зависит величина третьего члена. [43]
В результате внутримолекулярной протонизации амидного азота в Т - З - фен - ОСНз, которая может возникнуть в результате образования водородной связи с гидроксильной группой, находящейся в положении 5, уменьшается ря-с. Зй-орбитами атакуется 5 -гидроксиль-ной группой. Нуклеофильный характер последней из-за образования водородной связи с азотом значительно больше, чем в спиртах. [44]
Объясняется это протонизацией водорода. [45]
Страницы: 1 2 3 4