Протонирование - кислород
Cтраница 1
Протонирование кислорода, хотя и невыгодно, но необратимо ведет ( при данных условиях) к образованию продукта конденсации. [1]
Протонирование кислорода карбонильной группы ацетона облегчает отрыв протона от СН3 - группы сопряженным основанием. [2]
При протонировании кислорода, хотя оно и облегчает атаку нуклеофильным реагентом, окончательное вытеснение амина и завершение реакции могут произойти только после переноса протона с кислорода на азот. Протонирование азота непосредственно активирует уходящий амин. Однако главной причиной высокой реакционной способности ацетилимидазола и ацетилимидазолиевого иона является прежде всего упомянутая выше относительно небольшая резонансная стабилизация этих соединений по сравнению с обычными амидами. [3]
Процесс включает быстрое равновесное Протонирование глико-зидного кислорода, медленный гетеролиз с образованием циклического карбоний-иона, который существует в конформации полукресла. [4]
Следовательно, протонирование кислорода карбонильной группы производных карбоновых кислот сводится к смещению я-электронного облака карбонильной группы от реакционного центра. В случае сопряжения заместителей с карбонильной группой протонирование карбонильного кислорода должно приводить к уменьшению подобного сопряжения. [5]
Реакция начинается с протонирования кислорода окисного кольца. Этим объясняется тиракс-стереоселективность раскрытия а-окисного кольца. [6]
Реакция начинается с протонирования кислорода окисного кольца. Этим объясняется пгракс-стереоселективность раскрытия а-окисного кольца. [7]
Константа скорости ks реакции протонирования кислорода велика и не появляется в уравнениях скорости. [8]
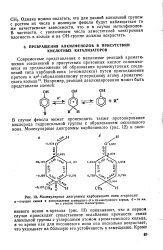 |
Молекулярные диаграммы карбониевого иона п-крезола. [9] |
В случае фенола может происходить также протонирование кислорода гидроксильной группы с образованием оксониевого иона. [10]
Возможно, при расщеплении пептидоглюкана бактериальной оболочки элементарный акт протонирования гликозидного кислорода кислотной группы активного центра фермента перестает быть лимитирующей стадией гидролиза в отличие от низкомолекулярных субстратов, так что эта стадия уже не проявляется в рН - зависимости константы скорости расщепления бактериальной клеточной стенки. [11]
Ациклический механизм, предложенный Армстронгом и Глове-ром [103], включает Протонирование циклического кислорода и разрыв пиранозного кольца по Ci-О - связи с образованием ациклического карбоний-иона. [12]
Протонирование азота ( в) привело бы к исчезновению резонансной стабилизации, тогда как протонирование кислорода не привело бы к этому ( структуры г и д), и, следовательно, система с протонированным кислородом должна быть более устойчивой. [13]
Механизм кислотного гидролиза гликопиранозидов по существу обратен механизму их образования по методу Фишера и включает протонирование гликозидного кислорода и расщепление гликозид-ной С-0-связи с образованием катиона ( 97), который затем атакуется молекулой воды. Однако не могут быть полностью исключены и другие пути гидролиза, включающие образование ациклических промежуточных продуктов. В случае грет-бутилгликозидов преимущественно расщепляется связь кислород - - агликон из-за большей стабильности rper - бутилкарбениевого иона, что приводит к значительному ( более чем в 500 раз) увеличению скорости гидролиза по сравнению с н-алкилгликозидами. [14]
В этой схеме, как ив схеме Бантона, для пиранозидов первая стадия заключается в протонировании кислорода замещенного полуацетального гидроксила. Далее к протонированному гликозиду присоединяется вода и, наконец, при отщеплении спирта и протона освобождается сахар. [15]
Страницы: 1 2 3