Процесс - ионизация - металл
Cтраница 2
Пассивная пленка или адсорбционный слой, тормозящие процесс ионизации металла и сообщающие ему свойства инертного электрода, сами в электрохимическом отношении нередко довольно неустойчивые образования. Сдвиг потенциала в отрицательную сторону может привести к разрушению пленки, к десорбции кислорода и к переходу металла в растворимое, активное состояние. Чрезмерное же повышение анодного потенциала не ликвидирует пленки на поверхности, но зато в некоторых случаях значительно ускоряет ее растворение, благодаря чему скорость ионизации металла также растет. [16]
 |
Строение монослоя из ионов хромата на железе ( по Зрит-леру. [17] |
По мнению И. Л. Розен-фельда [41], основное торможение процесса ионизации металла происходит в результате образования первичной адсорбционной пленки, в то время как роль вторичной фазовой пленки сводится к механической изоляции части поверхности от воздействия раствора. [18]
Этот процесс может проходить там же, где протекает процесс ионизации металла. [19]
Уменьшению концентрации ионов циана у поверхности катода должен способствовать также процесс ионизации металлов, который, как отмечалось выше, протекает в исследованных растворах со значительной скоростью. [20]
Уравнение ( 112 1) показывает, что зависимость скорости процесса ионизации металла от потенциала электрода отличается одной особенностью от аналогичной зависимости процессов разряда ионов металла или ионизации кислорода на катоде. В последних случаях, как известно, сила тока стремится к некоторому предельному значению, обусловленному тем, что максимальная скорость диффузии достигается тогда, когда концентрация восстанавливающих веществ на катоде равна нулю. [21]
Таким образом, явление пассивности состоит в замедлении или полном прекращении процесса ионизации металлов вследствие изменения заряда и свойств поверхности, вызванных образованием на ней адсорбционных или фазовых слоев окислов. [22]
Таким образом, явление пассивности состоит в повышении перенапряжения или замедлении процесса ионизации металлов вследствие изменения заряда и свойств поверхности, вызванных образованием на ней адсорбционных или фазовых слоев окислов. Часто полагают, что основное различие между адсорбционной и пленочной теориями сводится к вопросу о количестве пассивирующего окислителя или форме его существования на поверхности. [23]
Из выражения ( 102 1) можно вывести уравнение для перенапряжения процесса ионизации металла, которое определяется как разница между потенциалом анода при данной плотности тока и равновесным потенциалом металла в этом же растворе: t a р - сра - Анодному перенапряжению при этом везде приписывается положительное значение. [24]
Отмечается, что исследованные алкил - и арилмеркаптаны в большей степени тормозят процесс ионизации металла. [25]
При аэрации природных сред или периодическом воздействии на металл электролита и атмосферного воздуха процесс ионизации металлов с переменной валентностью продолжается до достижения металлом предельной валентности. [26]
При анодной поляризации меди, по данным Есина [66], замедленной стадией также является процесс ионизации металла, Эршлер 167 ] тоже предполагает, что растворение платины происходит по механизму замедленного разряда. [27]
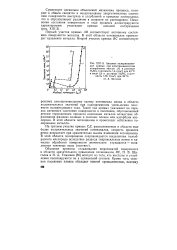
Такой ход кривых указывает на переход активного состояния поверхности в пассивное, обусловленный резким торможением процесса ионизации металла вследствие образования фазовых солевых и окисных пленок или адсорбции кислорода. В этой области потенциалов и происходит собственно полирование металла. [29]
Поскольку ток обмена для системы металл - раствор имеет конечную величину, то, следовательно, процессы ионизации металла и разряда его ионов также протекают с конечной скоростью. Для выяснения кинетических закономерностей этих процессов необходимо найти экспериментальным путем зависимость их скоростей от потенциала, концентраций реагирующих частиц и строения двойного слоя. [30]
Страницы: 1 2 3 4