Процесс - ионизация - металл
Cтраница 4
В электролите, состоящем из 30 8 г / л AgCN и 21 г. л KCNCB06, растворимость неполяризованного серебряного электрода при комнатной температуре составляет 4 3 - 10 - 3 г / см2 в сутки. Естественно, что процесс ионизации металла приводит к повышению концентрации AgCN у поверхности катода и тем самым может способствовать образованию пассивирующей пленки. [46]
При протекании коррозионного разрушения процесс окисления металла сопряжен с процессом восстановления окислителя из коррозионноактивной среды. В простейшем случае процессу ионизации металла соответствует процесс восстановления одного окислителя. Область, в которой будет находиться потенциал корродирующего металла, зависит от природы металла ( сплава) и окислителя. [47]
На кривой имеется четыре характерных участка, отвечающих различным электрохимическим процессам. Участок АБВ характеризует изменение скорости процесса ионизации металла от потенциала в условиях, когда железный анод находится в активном состоянии. В точке В электрод, несмотря на то, что поверхность железа остается блестящей, становится пассивным и перестает растворяться. В пассивной области плотность тока в значительной области потенциалов ГД не зависит от потенциала анода. Четвертый участок ДЕ характеризует, таким образом, процесс выделения кислорода. [48]
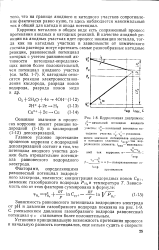 |
Коррозионная диаграмма. [49] |
В качестве анодной реакции на анодных участках идет процесс ионизации металла, тогда как на катодных участках в зависимости от химического состава раствора могут протекать самые разнообразные катодные реакции, ра. [50]
Страницы: 1 2 3 4