Процесс - окисление - железо
Cтраница 2
При небольшой скорости процесса окисления железа образование гидрата закиси железа происходит медленнее, чем его окисление в гидрат окиси, вследствие чего в реакционной среде гидрат закиси отсутствует, и получение продуктов присоединения Fe ( OH) 2 Fe ( OH) 3 - невозможно. Поэтому при окислении металлического железа кислородом воздуха может происходить только один окисел - гидрат окиси железа. [16]
При небольшой скорости процесса окисления железа образование гидрата закиси железа происходит медленнее, чем его окисление в гидрат окиси, вследствие чего в реакционной среде гидрат закиси отсутствует, и получение продуктов присоединения Fe ( OH) 2 Fe ( OH) 3 невозможно. Поэтому при окислении металлического железа кислородом воздуха может получаться только один окисел - гидрат окиси железа. [17]
 |
Зависимость основных составляющих шлака от разрезаемой толщины стали и скорости резки. [18] |
Изложенные представления о процессе окисления железа справедливы для сплавов железа и структурных составляющих сплавов, температура плавления окислов которых ниже или равна температуре воспламенения железа и кислорода. В противном случае, как было отмечено, на поверхности жидкого металла образуется твердая пленка окислов, непроницаемая для кислорода и препятствующая дальнейшему окислению железа. [19]
Предполагают, что в процессе окисления железа возникают его активные формы ( наиболее вероятно - соединения пятивалентного железа), которые, собственно, и окисляют хлориды до свободного хлора. Это достигается введением в раствор солей двухвалентного марганца и смеси фосфорной и серной кислот. По-видимому, Мп ( II) играет роль своеобразного катализатора или регулятора химической реакции между перманганатом и двухвалентным железом и направляет ее по строго определенному пути. [20]
Исследованиями ТатНИПИнефть установлено, что процесс окисления железа происходит медленно. При этом рН воды не изменяется. [21]
Вопреки этому В. О. Лукашевичем экспериментально доказана ступенчатость процесса окисления железа нитросоединениями. Встряхиванием на холоду тонкого порошка железа с нитробензолом в присутствии разбавленного раствора железного купороса он получил темиозеленый осадок сравнительно медленно окисляющегося гидрата закиси железа; при нагревании окисление его проходит быстро. [22]
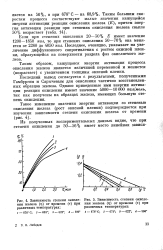 |
Зависимость степени окисле - [ IMAGE ] Зависимость степени окисления железа ( TJ от времени ( т при ния железа ( г от времени ( т при различных температурах. различных температурах. [23] |
Таким образом, кажущаяся энергия активации процесса окисления железа является величиной переменной и меняется ( возрастает) с увеличением толщины окисной пленки. [24]
Вопреки этому В. О. Лукашевичем экспериментально доказана ступенчатость процесса окисления железа нитросоединениями. [25]
Одним из основных условий, обеспечивающих непрерывность процесса окисления железа при резке, является равенство тепло-вложений и теплопотерь в энергетическом балансе процесса. Если теплопотери превышают тепловложения, нарушаются необходимые температурные условия на границах раздела фаз, и процесс окисления прерывается. [26]
Участие углекислого газа или окиси углерода в процессе окисления железа доказывает наличие в окисной пленке углерода. [27]
Каталитическое действие щелочи с образованием промежуточных соединений облегчает процесс окисления железа и разрушения имеющихся на его поверхности пленок. Так как окисление металла происходит здесь за счет разложения воды, то в результате реакции должно наблюдаться увеличение щелочности. В отсутствие кислорода процесс растворения протекает довольно быстро ( рис. 2 - 5) и сопровождается значительным выделением водорода. [28]
Роль электролитов при этом процессе выражается в ускорении процесса окисления железа при влажной коррозии вследствие увеличения электропроводности раствора, но сами они при реакции восстановления не расходуются, являясь, таким образом, лишь катализаторами. [29]
Процесс обезуглероживания стали и чугуна происходит одновременно с процессом окисления железа, содержащегося в них. При этом скорость обезуглероживания может превышать скорость окисления. [30]
Страницы: 1 2 3 4