Процесс - окисление - железо
Cтраница 4
Из (21.50), (21.51) видно, что время защитного действия зависит от размеров зоны зарядки пласта, расхода откачки, а также от параметров, характеризующих процесс адсорбции кислорода и процесс окисления железа. При этом с ростом объема закачки в пласт аэрированной воды и количества адсорбированного кислорода tQ увеличивается, а с повышением расхода откачки снижается; при прочих равных условиях время защитного действия уменьшается с повышением содержания железа в подземной воде. [46]
При окислении закисного железа кислородом из воздуха или пресной воды железо переходит к окисную форму и выпадает в осадок. Процесс окисления железа протекает сравнительно медленно и может заканчиваться после очистки воды. [47]
Из рисунков видно, что при нагревании железа до температуры ниже 570 на его поверхности образуется два окисла: гематит ( Ре2Оз) и магнетит ( FegOJ. Процесс окисления железа в этих условиях протекает медленно в связи с пониженной скоростью диффузии атомов железа и кислорода в указанном интервале температур. [48]
При этих условиях процесс окисления железа ( II) протекает очень медленно. [49]
Как видно из этого уравнения, кажущаяся энергия активации процесса окисления Ст. По данным [12], энергия активации процесса окисления железа на воздухе в интервале температур 242 - 375 С составляет 21 000 кал. [50]
Кислота, обычно соляная, добавляемая в небольшом количестве, требуется для образования соли двухвалентного железа. Раствор ее играет роль электролита в процессе окисления железа кислородом воды с выделением водорода, восстанавливающего нитробензол. [52]
Кислота, обычно соляная, добавляемая в небольшом количестве, требуется для образования соли двухвалентного железа. Раствор ее играет роль электролита в процессе окисления железа кислородом водь: с выделением водорода, восстанавливающего нитробензол. [54]
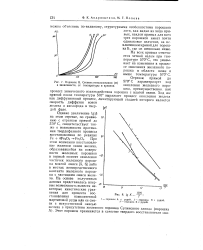 |
Порошок В. Степень использования ( т в зависимости, от температуры и времени. [55] |
С характеризует ход окисления железного порошка, преимущественно как процесс химического взаимодействия порошка с влагой окиси. Ход же прямой после температуры 570 выражает процесс окисления железа как диффузионный процесс, лимитирующей стадией которого является скорость диффузии ионов железа и кислорода в твер - л дои фазе. [56]
Указанное явление усугубляется еще тем, что Гамбург и Сарычев изучали окисление не чистого железа, а частично окисленных ( на 50 %) образцов железа. Поэтому полученные ими уравнения и выводы нельзя перенести на процесс окисления железа и образцов железа, имеющих иную степень окисления. В последнем случае будут, очевидно, другие соотношения между линейным и параболическим участками кривых, характеризующих изменение веса образцов с течением времени. [57]
Страницы: 1 2 3 4

